
12. По медной проволоке с площадью поперечного сечения 0,01 см2 проходит ток I = 20А. Оценить скорость дрейфа электронов в электрическом поле и сравнить ее со скоростью Ферми при Т=0 К. Cчитать эффективную массу равной массе свободного электрона. (Решение → 21775)
Заказ №39111
12. По медной проволоке с площадью поперечного сечения 0,01 см2 проходит ток I = 20А. Оценить скорость дрейфа электронов в электрическом поле и сравнить ее со скоростью Ферми при Т=0 К. Cчитать эффективную массу равной массе свободного электрона. Дано: S=0,01 см2=10-6 м 2 I = 20А m=9,1∙10-31 кг Найти: vd, vF
Решение.
При наложении внешнего электрического поля в металлическом проводнике кроме теплового движения электронов возникает их упорядоченное движение (дрейф), то есть электрический ток. Среднюю скорость d дрейфа можно оценить из следующих соображений. За интервал времени Δt через поперечное сечение S проводника пройдут все электроны, находившиеся в объеме d S t Число таких электронов равно d nS t , где n – средняя концентрация свободных электронов, примерно равная числу атомов в единице объема металлического проводника. Через сечение проводника за время Δt пройдет заряд d q enS t . Отсюда следует: d q I enS t или d I enS Плотность меди o A m N Nm V V VN , где - молярная масса, NA- число Авогадро.

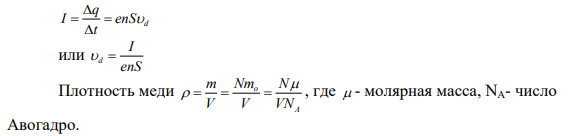

- 25г медного купороса CuSO4·5H2O растворили в 175г воды. Определите процентную концентрацию раствора в расчете на безводную соль. б) В 500мл раствора, плотность которого 1,03 г/мл, растворено 120г уксусной кислоты. Определите процентную и молярную концентрацию раствора.
- Определите класс указанных соединений; составьте молекулярные и ионные уравнения возможных реакций между этими соединениями с водой, серной кислотой и гидроксидом натрия. 9 Be(OH)2, HNO2, SO2, Ca(HSO3)2, SnOHNO3
- Располагая собственным капиталом в 60 тыс. руб., предприятие решило привлечь заемный капитал для финансирования капвложений. Необходимо определить, при какой структуре капитала будет достигнут наивысший уровень рентабельности капитала и собственного капитала предприятия.
- ЭДС электрохимической цепи, составленной из стеклянного и насыщенного хлорсеребряного электродов, опущенных в мочу при 310 К, равна 0,335 В. Константа стеклянного электрода равна 0,238 В. pH мочи равен:
- Проанализируйте изменение объема реализованной продукции ( V ) под влиянием структурных изменений в дневной продаже ее видов ( i ) (i – номенклатурная позиция).
- Равновесие в системе: А(г) + В(г) 2С(г) ) установилось при следующих концентрациях: [В ]и [С],моль/л. Определить исходную концентрацию вещества [В]0 и константу равновесия, если исходная концентрация вещества А равна [А]0 моль/л № зад. Концентрация, моль/л
- Дать общую характеристику одноосновным карбоновым кислотам. Напишите структурную формулу акриловой (простейшей непредельной одноосновной карбоновой) кислоты и уравнение реакции взаимодействия этой кислоты с метиловым спиртом. Напишите структурную формулу образовавшегося продукта, составьте схему его полимеризации.
- При полном сгорании 2 кг октана выделилось 90 МДж тепла Вычислить энтальпию образования октана
- Составьте уравнения реакций окисления металлов, используя значения окислительно-восстановительных потенциалов металлов, кислорода и водорода в различных средах (табл. П.2, П.3). Значения потенциалов разбавленной и концентрированной азотной и концентрированной серной кислот примите равными 1 В. Сделайте вывод о практической устойчивости металла в данной среде.
- По данным локомотивного депо проанализируйте изменение затрат на материалы ( En ) для деповского ремонта локомотивов ВЛ10 под влиянием структурных сдвигов по видам ремонтов ( i ) и изменений в затратах материалов на каждый вид ремонта ( Цi ) (i – вид ремонта).
- Вычислите процентную концентрацию водного раствора метанола СН3ОН, температура кристаллизации которого –2,790С.
- Составьте электронно-ионные схемы и молекулярные уравнения ОВР. Укажите окислитель и восстановитель. 2.9. а) SnCl2 + K2Cr2O7 + HCl Sn4+, Cr3+ б) I2 + Na2SO3 + H2O I ¯ , SO4 2-
- Задание 3 Рассчитать объем реактора полного смешения непрерывного действия, если в нем протекает химическая реакция А→В. Исходная концентрация вещества А 0,5 моль/л, а степень превращения 0,9. Объемный расход реакционной массы 30 л/мин. Константа скорости протекающей реакции 0,5 мин-1 .
- При потенциометрическом титровании 15 см3 крови раствором с С (НС1) = 0,12 моль/дм3 получен скачок, которому соответствует объём кислоты 0,63 см3 . Концентрация оснований в крови в ммоль/дм3 равна:
