
Дано уравнение реакции (см. вариант 18 в табл. 3) 1. Найдите в прил.1 стандартные энтальпии образования ∆H°(298° K) и стандартные энтропии S° (298° K) для всех веществ, участвующих в реакции. (Решение → 34438)
Заказ №38812
Дано уравнение реакции (см. вариант 18 в табл. 3) 1. Найдите в прил.1 стандартные энтальпии образования ∆H°(298° K) и стандартные энтропии S° (298° K) для всех веществ, участвующих в реакции. 2. Вычислите изменения энтальпии и энтропии при протекании прямой реакции в стандартных условиях. Сделайте вывод, экзо- или эндотермическая данная реакция и объясните знак ∆ S. 3. Вычислите энергию Гиббса прямой реакции в стандартных условиях ∆G° (298° К) и установите направление самопроизвольного протекания реакции. 4. Определите температуру, при которой реакция находится в равновесии. 5. Рассчитайте ∆G° при Т=Тр – 100 и Т= Тр + 100 и постройте график зависимости ∆G° и Т. Определите область температур самопроизвольного протекания реакции- и веществовосстановитель. 6. Вычислите значение константы равновесия (К) для температур: Т=Тр, Т= Tp -100, T=Tp – 100. Сделайте вывод о влиянии температуры на величину К и на смещение равновесия. 7.Как изменится энтропия, если к продуктам, полученным в результате реакции добавить 1 моль N2 ?
Решение:
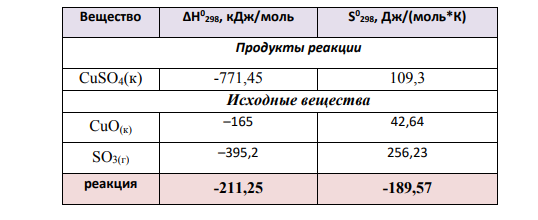
1. В таблице указаны стандартные энтальпии образования ∆H°(298° K) и стандартные энтропии S° (298° K) для всех веществ, участвующих в реакции. CuO(к)+SO3(г)=CuSO4 Таблица 3.1 – Вычисление энтальпии и энтропии реакции при стандартных условиях Вещество ΔН0 298, кДж/моль S 0 298, Дж/(моль*К) Продукты реакции CuSO4(к) -771,45 109,3 Исходные вещества CuO(к) –165 42,64 SO3(г) –395,2 256,23 реакция -211,25 -189,57 185 2. Энтальпия, как и внутренняя энергия, является функцией состояния; ее изменение (∆H) определяется только начальными и конечными состояниями системы и не зависит от пути перехода. Нетрудно видеть, что теплота реакции в изохорно-изотермическом процессе (V=const, T=const), при котором ∆V=0, равна изменению внутренней энергии системы: QV = ∆U. Теплоты химических процессов, протекающих при p, T=const и V, T = const, называют тепловыми эффектами. При экзотермических реакциях энтальпия системы уменьшается и ∆H0 (Н2>Н1). В дальнейшем тепловые эффекты всюду выражается через ∆rH. Термохимические расчеты основаны на законе Гесса (1840): тепловой эффект реакции зависит только от природы и физического состояния исходных веществ и конечных продуктов, но не зависит от пути перехода. Часто в термохимических расчетах применяют следствие из закона Гесса: тепловой эффект реакции (∆rH) равен сумме теплот образования (∆fH) продуктов реакции за вычетом суммы теплот образования исходных веществ с учетом коэффициентов перед формулами этих веществ в уравнении реакции ∆rH = ∑ ni∆fHпрод – ∑ nj∆fHисх Стандартная энтальпия образования ΔНобр – теплота, выделяемая или поглощаемая при образовании 1 моль вещества из простых веществ, его составляющих, при стандартных условиях. Для данной реакции CuO(к)+SO3(г)=CuSO4 ∆rH = ∑ ni∆fHпрод – ∑ nj∆fHисх=-211,25 кДж/моль (см. табл.3.1) ∆Hr 0, или H – T S < 0. Значение этой функции (ее знак): G = H – T S 186 и определяет направление процесса. Функция состояния системы G называется энергией Гиббса, или изобарноизотермическим потенциалом, или свободной энергией (устар.) системы. В системе в качестве самопроизвольного возможен только тот процесс, в результате которого энергия Гиббса системы уменьшается, G < 0. Это одно из основных уравнений химической термодинамики, т.к. связывает возможность протекания химической реакции в системе с происходящими при этом изменениями H и S. На основании стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ вычислим ΔG 0 298 реакции, протекающей по уравнению. Вся система является газообразной, поэтому при расчете энергии Гиббса будем учитывать все элементы системы. Для расчета используем теплоты образования и энтропий веществ при стандартных условиях (Т=298К, р=1.13*105Па). Вычисления производим, используя следствия закона Гесса.





- Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) KHCO3 и H2SO4; б) Zn(OH)2 и NaOH; 6) CaCL2uAgNO2.
- Укажите принципиальное отличие хинина от хинидина. Напишите схему реакции подлинности ФС на хинин, в результате которой появляется зеленое окрашивание.
- Предприятие приборостроения реализует проект модернизации производства. Для его осуществления необходимо осуществить следующие затраты: 1 год – 2400 млн. руб., 2 год – 1750 млн. руб., 3 год - 1250 млн. руб.
- Сформулируйте кинетический и термодинамический подходы к состоянию равновесия. Напишите выражения констант равновесия следующих реакций: NH3(г) + НCl(г) NH4Cl(к) 2Н2(г) + СO(г) СН3ОН(г)
- Организации была предоставлена отсрочка по уплате налога. В качестве обеспечительной меры налоговый орган заключил с исполнительным директором данной организации договор поручительства. Вскоре после заключения указанного договора на очередном собрании акционеров было принято решение о назначении нового исполнительного директора.
- Напишите уравнения состояния идеального и реального газов. Объясните физический смысл поправок, введенных в уравнение Ван-дер-Ваальса.
- Прокурору Ярославской области стало известно, что КУМИ Переславского муниципального района заключило 59 договор купли-продажи земельного участка, находящегося в государственной собственности, с региональной общественной организацией «Клуб хранителей традиций русской охоты» на основании постановления главы Переславского муниципального района «О предоставлении в собственность земельного участка РОО «Клуб хранителей традиций русской охоты». Площадь участка — 20 000 кв. м, адрес: Ярославская область, Переславский район. Цена по договору купли-продажи составила 111 000 (сто одиннадцать тысяч) рублей.
- Для создания ландшафтного заказника постановлением органа исполнительной власти субъекта РФ было принято решение об изъятии у фермера К. 20 га пахотных угодий, принадлежащих ему на праве собственности. В судебном заседании К. пояснил, что считает принятие данного решения незаконным по двум основаниям: во-первых, не была соблюдена обязательная процедура резервирования земельного участка; во-вторых, вид использования земельного участка — сенокошение и пастьба скота — является традиционным для данной местности, не отразится на её рельефе и, следовательно, не противоречит целям создания заказника
- P t=20°C в 1л насыщенного раствора йодида серебра AgI содержится 0.044г соли. Вычислите произведение растворимости этой соли.
- Які реакції називаються реакціями обміну?
- Рассчитайте, как изменятся скорости прямой и обратной реакций в равновесной системе 2С2Н6(г) + 7О2(г) = 4СО2(г) + 6Н2О(г) если давление увеличить в 3 раза? В каком направлении сместится равновесие?
- Рассчитайте производственную мощность механического участка однономенклатурного производства, учитывая данные таблицы
- Характеристика витамина В9 (фолиевой кислоты), биологическая роль.
- Материальные затраты предприятия на производство продукции за месяц составили 350 тыс. руб., заработная плата работников – 53 тыс. руб., амортизационные отчисления – 16 тыс. руб., прочие расходы – 23 тыс. руб. Выручка от реализации продукции составила 682 тыс. руб.
