
Ирина Эланс
На основании значений констант скоростей реакции при двух температурах определить: энергию активации, константу скорости при температуре T3, температурный коэффициент скорости и количество вещества, израсходованного за (Решение → 45022)
Заказ №76445
На основании значений констант скоростей реакции при двух температурах определить: энергию активации, константу скорости при температуре T3, температурный коэффициент скорости и количество вещества, израсходованного за время τ, если начальные концентрации равны C0. Принять, что порядок реакции и молекулярность совпадают. Размерность констант соответственно мин -1 (кмоль/м3 ) -1 (для реакции II порядка).
Решение:
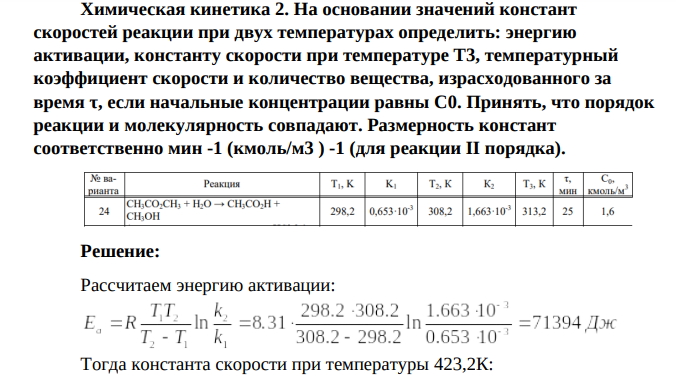
Рассчитаем энергию активации: Тогда константа скорости при температуры 423,2К:

- Для указанной реакции вычислите ΔН298, ΔGТ, КТ равн. На основе расчетов сделайте вывод о тепловом эффекте процесса, его термодинамической возможности при заданных температурах и положения равновесия
- С позиций метода валентных связей (МВС) объясните строение предложенных молекул. Укажите тип гибридизации центрального атома, изобразите перекрывание орбиталей
- Рассчитайте расход электроэнергии для покрытия слоем цинка 35 мкм поверхности изделия общей площадью 5м2 , учитывая, что выход по току равен 0,68, а оцинкование проводится из раствора
- Составьте схему, напишите уравнения электродных процессов элемента, состоящую из никелевой и свинцовой пластины, опущенных в раствор, содержащий собственные ионы
- Какой объем азота (н.у.) и сколько кг карбида кальция необходимо для получения 1 т технического цианамида кальция, содержащего 69 % CaCN2
- Напишите уравнение окислительно-восстановительного процесса, составив электронно-ионный баланс: KNO2 + HI + H2SO4 → Определите молярную массу
- Какую реакцию имеют растворы Na2SO3 и NaHSO3? Вычислите константу гидролиза для сульфит- и гидросульфит-ионов
- Составьте схему, напишите электронные уравнения электродных процессов н вычислите ЭДС гальванического элемента, состоящего из свинцовой и магниевой пластин, опущенных в растворы своих солей с концентрацией
- Определить в каком направлении могут самопроизвольно протекать реакции. Ответ подтвердить расчетом. NaNO2 + KMnO4 + H2SO4 NaNO3 + MnSO4 ++ K2SO4 + Н2О
- Уравнять методом электронного баланса Мn(ОН)2 + Сl2 + КОН = МnО2 + KCl + Н2О
- Учитывая, что гидролиз идет по первой ступени, вычислите константу, степень гидролиза и pH в водном растворе соли по следующим данным: 24 NH4NO3 0,1M
- Чему равна степень диссоциации ортофосфата натрия в 0,1 моль/л растворе, кипящем при 100,17°С. Плотность раствора 1,007 г/см3
- При 50°С давление пара над водой равно 12,30 кПа. Сколько граммов глицерина С3Н5(ОН)3 необходимо растворить в 460 г воды, чтобы понизить давление пара на 0,10 кПа
- Способы выражения состава растворов Рассчитайте: а) массовую долю растворенного вещества; б) молярную концентрацию
