
Определите характер связи в молекулах CsF, F2, BrCl, CaH2, NCl3 (Решение → 23395)
Заказ №38812
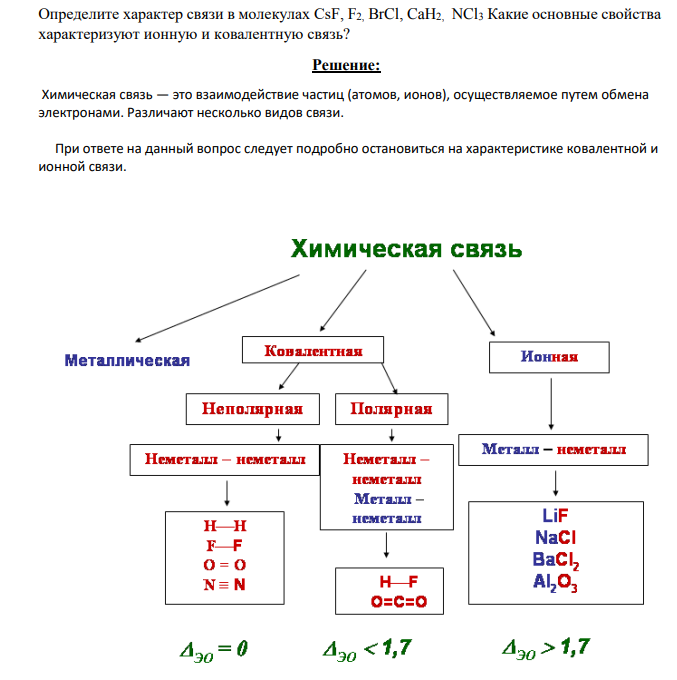
Определите характер связи в молекулах CsF, F2, BrCl, CaH2, NCl3 Какие основные свойства характеризуют ионную и ковалентную связь?
Решение:
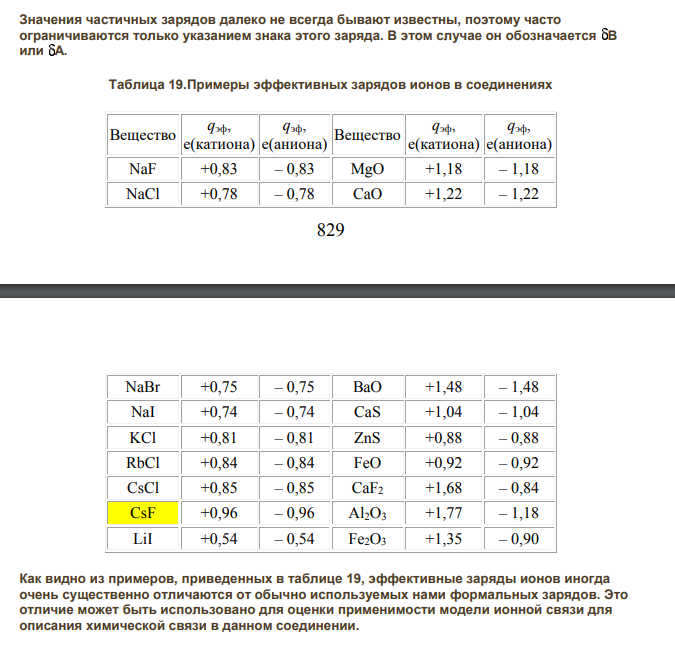
Химическая связь — это взаимодействие частиц (атомов, ионов), осуществляемое путем обмена электронами. Различают несколько видов связи. При ответе на данный вопрос следует подробно остановиться на характеристике ковалентной и ионной связи. Значения частичных зарядов далеко не всегда бывают известны, поэтому часто ограничиваются только указанием знака этого заряда. В этом случае он обозначается B или A. Таблица 19.Примеры эффективных зарядов ионов в соединениях Вещество qэф, е(катиона) qэф, е(аниона) Вещество qэф, е(катиона) qэф, е(аниона) NaF +0,83 – 0,83 MgO +1,18 – 1,18 NaCl +0,78 – 0,78 CaO +1,22 – 1,22 830 NaBr +0,75 – 0,75 BaO +1,48 – 1,48 NaI +0,74 – 0,74 CaS +1,04 – 1,04 KCl +0,81 – 0,81 ZnS +0,88 – 0,88 RbCl +0,84 – 0,84 FeO +0,92 – 0,92 CsCl +0,85 – 0,85 CaF2 +1,68 – 0,84 CsF +0,96 – 0,96 Al2O3 +1,77 – 1,18 LiI +0,54 – 0,54 Fe2O3 +1,35 – 0,90 Как видно из примеров, приведенных в таблице 19, эффективные заряды ионов иногда очень существенно отличаются от обычно используемых нами формальных зарядов. Это отличие может быть использовано для оценки применимости модели ионной связи для описания химической связи в данном соединении. Ковалентная связь образуется в результате обобществления электронов (с образованием общих электронных пар), которое происходит в ходе перекрывания электронных облаков. В образовании ковалентной связи участвуют электронные облака двух атомов. Различают две основные разновидности ковалентной связи: а) неполярную и б) полярную. а) Ковалентная неполярная связь образуется между атомами неметалла одного и того лее химического элемента. Такую связь имеют простые вещества, например О2; N2; C12. Можно привести схему образования молекулы водорода: (на схеме электроны обозначены точками). б) Ковалентная полярная связь образуется между атомами различных неметаллов. Схематично образование ковалентной полярной связи в молекуле НС1 можно изобразить так: Общая электронная плотность оказывается смещенной в сторону хлора, в результате чего на атоме хлора возникает частичный отрицательный заряд , а на атоме водорода — частичный положительный . Таким образом, молекула становится полярной: Ионной называется связь между ионами, т. е. заряженными частицами, образовавшимися из атома или группы атомов в результате присоединения или отдачи электронов Ионная связь характерна для солей и щелочей. Сущность ионной связи лучше рассмотреть на примере образования хлорида натрия. Натрий, как щелочной металл, склонен отдавать электрон, находящийся на внешнем электронном слое. Хлор же, наоборот, стремится присоединить к себе один электрон. В результате натрий отдает свой электрон хлору. В итоге образуются противоположно заряженные частицы — ионы Na+ и Сl-, которые притягиваются друг к другу. При ответе следует обратить внимание, что вещества, состоящие из ионов, образованы типичными металлами и неметаллами. Они представляют собой ионные кристаллические вещества, т. е. вещества, кристаллы которых образованы ионами, а не молекулами.


- Вариант 10. Определить бухгалтерские проводки, отразить операции по карточке счета 68. НДС.
- 2. Кот, принадлежащий К.Н. Заводской, сбежал на улицу и был подобран её соседкой Д.В. Остроуховой. Когда К.Н. Заводская обнаружила этот факт, она обратилась к Д.В. Остроуховой с требованием о возврате кота, на что получила категорически отказ со ссылкой на то, что право собственности ничем не подтверждено, а значит, кот присвоен ей как бесхозяйное имущество. Подумайте, как К.Н. Заводской доказать своё право собственности.
- Насыщенный раствор CaSO4 смешали с равным объёмом раствора, содержащего 0,0248 г (NH4)2C2O4 в 1л. Произойдёт ли образование осадка CaC2O4?
- Напишите уравнения, отражающие анодный и катодный процессы при электрохимической коррозии в указанных ниже системах: 9.5.9. Кадмированное железо в кислой среде при нарушении целостности покрытия
- Написать структурные формулы следующих соединений: А. 3,5 – диметилгексен – 2, Б. 3 – метилбутин -1, В. Пентадиен -2,3. Составьте структурные формулы двух изомеров соединения А и назовите их. Решение:
- Расходная норма исходного сырья в производстве товаров народного потребления составляет на предприятии в среднем 112 кг. на 10. 0 кг. готовой продукции. За сутки вырабатывается 127 тонн продукции. Время между поставками сырья 10 суток, возможна задержка на 2 суток,
- К раствору, содержащему в 1 л 0,02 моль иона CdI4 2- и 1 моль/л ионов Cd2+, прибавлен 0,1 моль твердого нитрата свинца (II). Выпадет ли осадок иодида свинца?
- Какие соединения получатся при действии на бутин-1 следующих реагентов: а) брома; б) хлористого водорода; в) воды (в присутствии серной кислоты и солей двухвалентной ртути)?
- Какое количество 95%-ной соды необходимо для устранения общей жесткости 1000 м3 , если 1 литр воды содержит по 1 мэкв. ионов кальция и магния ?
- Если цена за единицу продукции – 550 руб., переменные затраты на единицу продукции – 250 руб., постоянные затраты на весь объем производства – 950 000 руб. Определите количество единиц продукции, которые необходимо реализовать, чтобы достичь точки безубыточности?
- Задание 2 Численность населения страны на конец года составляла 143,3 млн. чел., в том числе в возрасте моложе трудоспособного – 23,6 млн. чел., трудоспособном – 87,1 млн. чел., старше трудоспособного – 32,4 млн. чел. Определить: 1) удельный вес населения трудоспособного возраста в общей численности населения: 557
- Вычислить рН 1 М раствора ванадата калия K3VO4, гидролизующегося по первой ступени, если K3(H3VO4) = 4 10-15
- Представлен денежный поток по 4-летнему инвестиционному проекту, предполагаемый уровень доходности – 19.50% годовых. Эффективна ли данная инвестиция? (NPV, IRR, P, MIRR, PPS, PPD, NTV) t
- Составьте уравнения реакций получения гидроксидов кальция, бериллия, бария. Каковы их свойства Как изменяются основные свойства гидроксидов в ряду: Be(OH)2Ca(OH)2Ba(OH)2?
