
Ирина Эланс
При амперометрическом титровании 15,00 мл раствора свинца титровали стандартным раствором Na2SO4 Т (Na2SO4) = 0,004387 г/мл при Е = 1,0 В получили следующие данные (Решение → 44165)
Заказ №65773
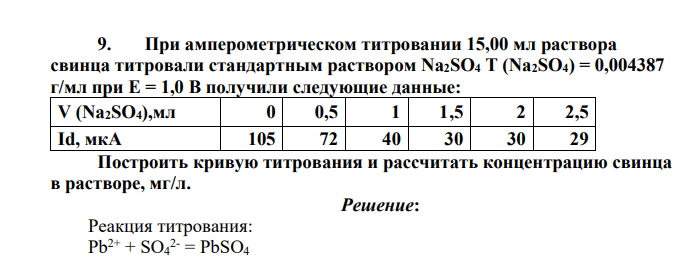
При амперометрическом титровании 15,00 мл раствора свинца титровали стандартным раствором Na2SO4 Т (Na2SO4) = 0,004387 г/мл при Е = 1,0 В получили следующие данные: V (Na2SO4),мл 0 0,5 1 1,5 2 2,5 Id, мкА 105 72 40 30 30 29 Построить кривую титрования и рассчитать концентрацию свинца в растворе, мг/л.
Решение:
Реакция титрования: Pb2+ + SO4 2- = PbSO4

- Навеску 0,1 г стали, содержащей медь, растворили в кислоте, после соответствующей обработки объем раствора в мерной колбе вместимостью 25 мл довели водой до метки. Аликвотную часть (5мл) этого раствора разбавили фоновым
- Рассчитайте количество прореагировавшего вещества при кулонометрическом определении при постоянном потенциале по приведенным данным. Процесс Количество вещества, выделившегося в кулонометре
- При титровании 15,00 мл раствора, содержащего К2СО3 0,1000 М раствором НСl, были получены следующие данные: V(мл) 9 10 10,5 11 11,5 pH 5,8 5,2 3,9 3 2,7 Постройте кривые потенциометрического титрования - интегральную
- Сделайте заключение о качестве таблеток аминофиллина по 0,15 г, если на титрование 0,1055 г (т.м.) порошка растертых таблеток израсходовалось 1,7 мл 0,1 моль л раствора хлористоводородной кислоты; средняя масса таблеток
- При количественном определении субстанции теофиллина на титрование навески массой 0,1902 г затрачено 10 мл 0,1 моль л раствора натрия гидроксида. Соответствует ли препарат требованиям ФС
- Какую навеску порошка состава Ацетилсалициловой кислоты 0,25 Фенобарбитала 0,03 нужно взять для определения, чтобы на тирование фенобарбитала израсходовалось 0,5 мл 0,1 моль л раствора натрия гидроксида
- Какой объем раствора натрия тиосульфата (0.1 моль/л) с К 1.0000. израсходуется при количественном определении лекарственной формы Раствор формальдегида, если в реакцию взяли 2.0 мл 1% раствора препарата и 20,0 мл раствора
- Из A и В электродов, погруженных в растворы их солей с концентрацией С(Аx+ ) и С(Вy+ ) составлен гальванический элемент. Составьте схему гальваническою элемента. Запишите процессы на электродах; уравнение реакции
- Сколько времени нужно осаждать никель на цилиндр диаметром 100 мм и высотой 50 мм, чтобы при силе тока 4 А нанести осадок толщиной 50 мкм? Выход по току никеля составляет 95%. Плотность никеля 8,9 г/см3
- Составить схему коррозионного элемента с нарушенным покрытием во влажном воздухе. Основа - Ge (Е° Ge2+/Ge = +0,01 В). Покрытие - As (Е° As3+/As = + 0,30 В); оно используется для облегчения пайки полупроводников
- Составить ГЭ, в котором оба электрода изготовлены из Cd и рассчитать ЭДС этого элемента
- Составить схему ГЭ из тех же металлов в растворе НСl. Записать процессы на электродах
- Составить схему гальванического элемента из Ag ( Е° = +0,80 В ) и Мn ( Е° = -1,18 В), опущенных в растворы их собственных солей с активностью ионов соответственно 10-3 и 10-2 моль/л. Записать процессы на электродах
- Вычислить энтальпию образования СО2, если известно, что при полном сгорании 1 г углерода выделяется 32,8 кДж тепла
