
При очистке реактора установки по производству соли (определяется номером варианта, столбец 2) часть продукта осталась не изъятой. Определить: 1.Концентрацию (СМ, Сm, Х, ω) раствора соли, если в реакторе её осталось 5 кг, а объём воды, необходимый для первичной отмывки реактора в 10 раз больше, чем для образования насыщенного раствора этой соли (S, г на 100 г воды, столбец 3) (Решение → 35696)
Заказ №38828
При очистке реактора установки по производству соли (определяется номером варианта, столбец 2) часть продукта осталась не изъятой.
Определить: 1.Концентрацию (СМ, Сm, Х, ω) раствора соли, если в реакторе её осталось 5 кг, а объём воды, необходимый для первичной отмывки реактора в 10 раз больше, чем для образования насыщенного раствора этой соли (S, г на 100 г воды, столбец 3). 2.При растворении соли в воде возможен её гидролиз. Запишите соответствующие уравнения процесса. Определите pH образовавшегося раствора (рН < 7, 𝑝𝐻 > 7, 𝑝𝐻 ≈ 7).
Таблица 4.1 Исходные данные № п/п Синтезируемая соль S, г 1 2 3 32 ZnCl2 367,3
Решение:
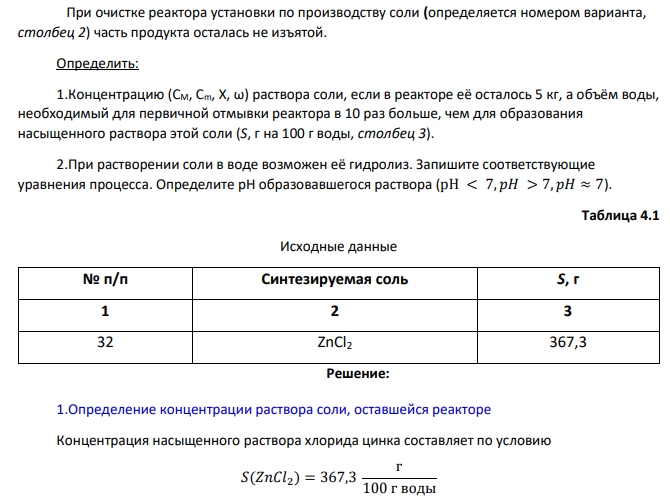
1.Определение концентрации раствора соли, оставшейся реакторе Концентрация насыщенного раствора хлорида цинка составляет по условию 𝑆(𝑍𝑛𝐶𝑙2 ) = 367,3 г 100 г воды Составим пропорцию для определения массы раствора 100 г воды------------------------------- 367,3 г (𝑍𝑛𝐶𝑙2 ) 1000 г воды---------------------------- х г (𝑍𝑛𝐶𝑙2 ) 𝑚(𝑍𝑛𝐶𝑙2) = 367,3 ∙ 1000 100 = 3 673 г Определяем массу воды, необходимую для промывки реактора из соотношения: 1000 г воды ---------------------------- 3 673 г х г воды ---------------------------------- 5000 г 𝑚𝐻2𝑂 = 1000 ∙ 5000 3 673 = 1 361 г Тогда масса раствора в реакторе 𝑚р−ра = 𝑚𝐻2𝑂 + 𝑚𝑍𝑛𝐶𝑙2 = 1361 + 5000 = 6 361г Массовая доля вещества в растворе w равна отношению массы растворенного вещества к массе раствора: 𝑤 = 𝑚𝑍𝑛𝐶𝑙2 𝑚р−ра ∙ 100% = 5000 6 361 ∙ 100% = 78,6 % 16 Молярная концентрация СM равна отношению числа молей растворенного вещества к объему раствора 𝐶𝑀 = 𝑚 𝑀 ∙ 𝑉р−ра = 𝑛 𝑉р−ра где n=m/M – число молей вещества, моль; 𝑛 = 𝑚/𝑀 mв-ва – масса растворенного вещества, г; 𝑚𝑍𝑛𝐶𝑙2 = 5 кг = 5000 г М – молярная масса вещества, г/моль; 𝑀𝑍𝑛𝐶𝑙2 = 65,37 + 2 ∙ 35,5 = 136,37 г/моль V – объем раствора, л; 𝑉 = 𝑚р−ра 𝜌 = 6361 1 = 6 361 мл = 6,361 л ρ – плотность раствора, г/мл; принимаем 𝜌 = 1 г см3



- По достижении совершеннолетия усыновленный стал доказывать, что будь он полновластным и способным к определению своей судьбы, он никогда не согласился бы с усыновлением. Служило ли такое утверждение основанием для принуждения домовладыки к его эманципации?
- Дано уравнение реакции (см. вариант 10 в табл. 3) 1. Найдите в прил.1 стандартные энтальпии образования ∆H°(298° K) и стандартные энтропии S° (298° K) для всех веществ, участвующих в реакции.
- Если в разбавленную серную кислоту опустить пластину из чистого железа, то выделение на ней водорода идет медленно и со временем почти прекращается. Почему прекращается?
- По данным таблицы 3 рассчитать: 1) коэффициент превышения ПДКсс по i-тому ингредиенту (qi); 2) ИЗА (Ii) отдельным ингредиентом; 3) номер i-того ингредиента в порядке уменьшения Ii (выполнить ранжирование загрязняющих веществ). Указать наиболее опасный из пяти ингредиентов.
- Вычислите степень окисления золота в соединении состава: 64,9% золота и 35,1% хлора. Молярная масса эквивалентов хлора 35,45 г/моль.
- Напишите реакции открытия иона свинца.
- Владелец небольшой фирмы имеет следующие ежегодные затраты: заработная плата наёмным работникам - 540 000 ден. ед., плата за аренду помещении 60 000 ден. ед., расходы на сырье 350 000 ден. ед.. На приобретение производственного оборудования он потратил 360 000 ден. ед. собственных средств, которые при ином размещении могли бы приносить ежегодный доход 36 000 ден. ед.
- Одно железное изделие покрыли никелем, другое – оловом. Обосновать, к какому типу относятся покрытия.
- Кинетические измерения показали, что реакция 2 2 2NO O 2NO имеет третий порядок. В начальный момент концентрации исходных веществ равны 0 NO и 2 0 O .
- Вычислите молярные массы эквивалентов и эквиваленты Р2О5 в реакциях, идущих по уравнениям: Р2О5 + 3MgO = Mg3(PO4)2; (1) P2O5 + MgO = Mg(PO3)2. (2)
- Какими реакциями можно отличить нитрит - ион от нитрата - иона (напишите уравнения качественных реакций).
- Определите значения всех квантовых чисел для электронов атомов а) лития: 6) бора: в) азота: г) фтора
- ФИО5 обратилась в суд с указанным иском, поддержанном ею в судебном заседании по тем основаниям, что ДД.ММ.ГГГГ она вступила в брак с ответчиком, от которого имеет двоих детей: ФИО3, ДД.ММ.ГГГГ года рождения и ФИО1, ДД.ММ.ГГГГ года рождения. Совместная жизнь с ответчиком не сложилась.
- При давлении 101,3 кПа и температуре 298,15 К вычислите изменение энергии Гиббса в результате реакции горения дициана: С ,N,(i) ♦ 20,(0 = 2СО, (г)♦ N, (г). Может ли эта реакция протекать самопроизвольно в закрытой системе при указанных условиях?
