
При решении задач этого раздела пользуйтесь таблицей 1 приложения. Для указанной реакции а) рассчитать стандартную энтальпию и энтропию; б) объяснить, какой из факторов: энтропийный или энтальпийный способствует самопроизвольному протеканию реакции в прямом направлении; в) в каком направлении (прямом или обратном) будет протекать реакция при 298К и 1000К; г) (Решение → 21798)
Заказ №39057
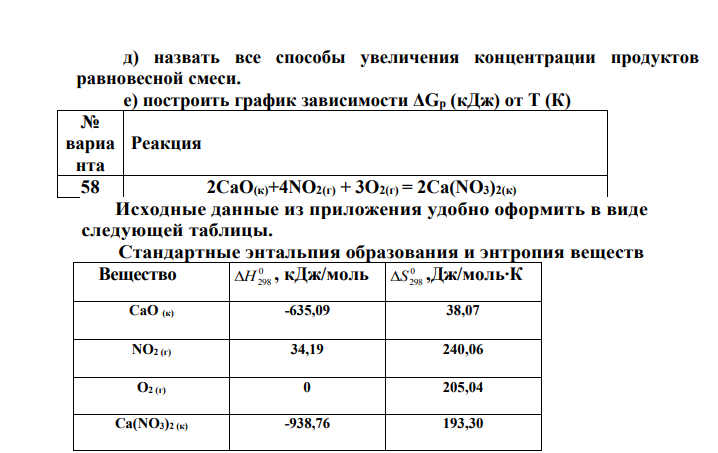
При решении задач этого раздела пользуйтесь таблицей 1 приложения. Для указанной реакции а) рассчитать стандартную энтальпию и энтропию; б) объяснить, какой из факторов: энтропийный или энтальпийный способствует самопроизвольному протеканию реакции в прямом направлении; в) в каком направлении (прямом или обратном) будет протекать реакция при 298К и 1000К; г) рассчитать температуру, при которой равновероятны оба процесса; д) назвать все способы увеличения концентрации продуктов равновесной смеси. е) построить график зависимости ΔGр (кДж) от Т (К) № вариа нта Реакция 58 2СаO(к)+4NO2(г) + 3O2(г) = 2Cа(NO3)2(к) Исходные данные из приложения удобно оформить в виде следующей таблицы. Стандартные энтальпия образования и энтропия веществ Вещество 0 Н298 , кДж/моль 0 S298 ,Дж/моль∙К CaO (к) -635,09 38,07 NO2 (г) 34,19 240,06 O2 (г) 0 205,04 Ca(NO3)2 (к) -938,76 193,30
Решение:
1. ( 0 Н298 )Х.Р. = (2f 0 Cа(NO3)2) - (3f 0 O2 + 4f 0 NO2 + 2f 0 СаO) = =(-938.76*2)-(0*3 + 34.19*4-635.09*2)= -744.1 кДж <0 – экзотермическая реакция - благоприятный фактор для протекания химической реакции, особенно при низких температурах. 2. ( 0 S298 )Х.Р. = (2fS 0 Cа(NO3)2) - (3fS 0 O2 + 4fS 0 NO2 + 2fS 0 СаO)= =193.3*2-(3*205.04+240.06*4+38.07*2)=-1264.9Дж/К= =-1.2649 кДж/моль<0. Прямая реакция сопровождается уменьшением энтропии, беспорядок в системе уменьшается - неблагоприятный фактор для протекания химической реакции в прямом направлении. 3. Рассчитываем стандартную энергию по уравнению: G0 298 = Н°298 - TS 0 298 ( G 0 298 )X.P. = -744.1-298* (1.2649) = -367.1 кДж<0



- Компании С и Д приняли решение об объединении деятельности. Следующие параметры характеризуют компании: Компания С выступает инициатором слияния. Оцените для компании С чистый эффект покупки (NPV), если экономия от масштаба позволит получать после слияния дополнительный денежный поток, текущая оценка которого равна 450 тыс. долл., и рассматривается вариант покупки компании Д за 800 тыс. долл.
- Можно ли признать достоверным вывод суда об умышленном причинении Шнуровым тяжкого вреда здоровью своей жене?
- Могут ли образоваться ковалентные связи перекрыванием атомных орбиталей: s и px, s и px, px и px, dxy и dxy? Ответ подтвердите рисунками. Укажите тип перекрывания атомных орбиталей.
- На титрование 15 мл муравьиной кислоты с титром 0,001150 г/мл расходуется 12,50 мл раствора гидроксида калия. Определить нормальную концентрацию и титр гидроксида калия.
- Задание 59 59. Методы атомно-эмиссионного анализа. Виды анализа, входящие в характеризуемую группу (классификации, краткая сравнительная характеристика).
- В закрытом сосуде 1 л воды взбалтывается при 15 оС с 0,5 л оксида азота N2О. Начальное давление оксида азота 750 мм рт. ст. Какой объем N2О, измеренный при нормальных условиях, растворится в воде?
- Задание 70 70. Люминесцентные методы анализа. Сущность характеризуемого метода анализа (основные понятия, законы и явления, лежащие в основе данного метода, история открытия, этапы развития).
- 6. Для нейтрализации 20,00 мл 0,2215 н. раствора HCl необходимо 21,40 мл раствора гидроксида бария, а 25,00 мл уксусной кислоты нейтрализуется 22,55 мл того же раствора. Определить нормальную концентрацию уксусной кислоты
- Для приведенных формул комплексных соединений: а) укажите внутреннюю и внешнюю координационные сферы, комплексообразователь и лиганды; б) определите заряд комплекса, степень окисления и координационное число комплексообразователя
- Задание Определите диаметр трубки капилляра, если хлороформ поднимается в ней на 19,3 мм. Поверхностное натяжение хлороформа равно 27,24·10-3 Н/м, плотность хлороформа составляет 1,48·103 кг/м3 .
- Предприятие привлекло три кредита: один долгосрочный - 1 000 000 руб. под 17% годовых, два краткосрочных – 550 000 руб. под 16% годовых и 268 268 700 000 руб. под 20% годовых. Кредиторская задолженность предприятия составляет 2 100 000 руб. Рассчитайте средневзвешенную стоимость заемных средств.
- Можно ли считать преступление продолжаемым?
- Оцените эффективность использования трудовых ресурсов в организации, определите влияние факторов на величину годовой выработки одного работника и объем выполненных ремонтных работ.
- Задание 37 37. В ходе анализа фракции смолы пиролиза на содержание стирола и толуола в исследуемую пробу массой 0,6781г добавили н-октан в качестве внутреннего стандарта массой 0,1389 г. Площадь пиков Sоктана- 49 мм ; Sстирола- 40 мм ; Sтолуола- 78 мм"
