
Вычислите температуру кристаллизации раствора мочевины (NH2)2CO, содержащего 5 г мочевины в 150 г воды. Криоскопическая константа воды 1,86°. (Решение → 26524)
заказ №38755
263.
Вычислите температуру кристаллизации раствора мочевины (NH2)2CO, содержащего 5 г мочевины в 150 г воды. Криоскопическая константа воды 1,86°.
Решение:
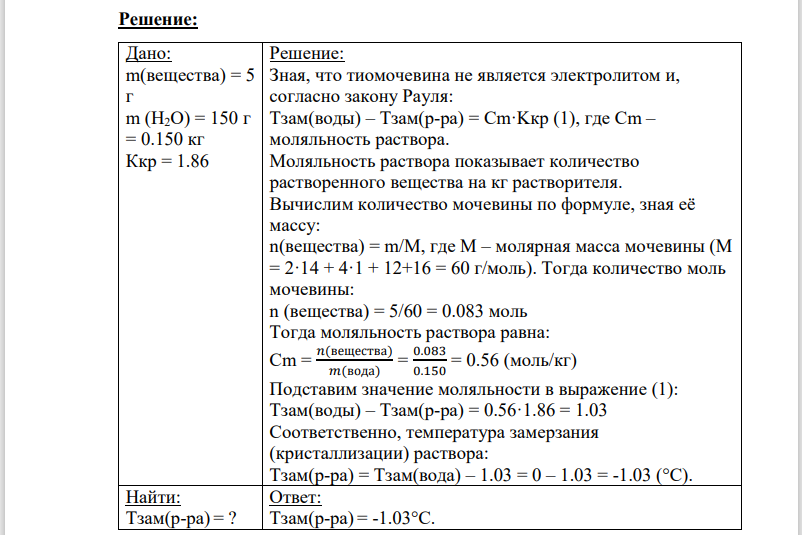
Дано: m(вещества) = 5 г m (H2O) = 150 г = 0.150 кг Ккр = 1.86
Решение: Зная, что тиомочевина не является электролитом и, согласно закону Рауля: Тзам(воды) – Тзам(р-ра) = Сm·Kкр (1), где Cm – моляльность раствора. Моляльность раствора показывает количество растворенного вещества на кг растворителя. Вычислим количество мочевины по формуле, зная её массу: n(вещества) = m/M, где М – молярная масса мочевины (М = 2·14 + 4·1 + 12+16 = 60 г/моль). Тогда количество моль мочевины: n (вещества) = 5/60 = 0.083 моль Тогда моляльность раствора равна: Cm = 𝑛(вещества) 𝑚(вода) = 0.083 0.150 = 0.56 (моль/кг) Подставим значение моляльности в выражение (1): Тзам(воды) – Тзам(р-ра) = 0.56·1.86 = 1.03 Соответственно, температура замерзания (кристаллизации) раствора: Тзам(р-ра) = Тзам(вода) – 1.03 = 0 – 1.03 = -1.03 (°С).
Найти: Тзам(р-ра) = ?
Ответ: Тзам(р-ра) = -1.03°С.


- Определите изменение фондоотдачи, фондовооруженности и производительности труда после внедрения автоматической линии, если до внедрения было произведено 200 тыс. шт. изделий, стоимость основных фондов – 200 млн руб., себестоимость одного изделия – 3000 руб., цена – 3500 руб.,
- Рассчитайте фактор реакции, молярную массу эквивалента, титр титранта по определяемому веществу при количественном определении стрептоцида (М.м. 172,21) броматометрическим методом (титранты 0,1 моль/л калия бромат и натрия тиосульфат). Дайте обоснование данному методу количественного определения.
- Предприятие рассматривает вопрос о целесообразности замены старых агрегатов на новые. Старое оборудование было куплено 5 лет назад за 1800000 руб. и может прослужить еще в течение 5 лет, после чего подлежит 524 списанию в связи с полным физическим износом. В настоящее время оно может быть продано за 900000 руб. Новое оборудование с нормативным сроком полезного использования 5 лет в настоящее время на рынке можно приобрести за 2400000 руб.
- Рассчитайте фактор реакции, молярную массу эквивалента, титр титранта по определяемому веществу при количественном определении парацетамола (М.м. 151,17) методом нитритометрии (титрант 0,1 моль/л раствора натрия нитрит). Дайте обоснование данному методу количественного определения.
- Требуется: 1) рассчитать маржинальный доход, долю маржинального дохода в выручке, прибыль; 2) оценить, производство какого изделия наиболее выгодно и наименее выгодно, исходя из приносимого каждым изделием маржинального дохода; 3) рассчитать критический объем производства.
- Рассчитайте фактор реакции, молярную массу эквивалента, титр титранта по определяемому веществу при количественном определении цинка сульфата (М.м. 287,54) трилонометрическим методом (титрант 0,05 М раствор трилона Б). Дайте обоснование данному методу количественного определения.
- В таблице представлены исходные данные производственной программы фирмы. Фирма действует в условиях совершенной конкуренции. Требуется: 1) рассчитать маржинальный доход, долю маржинального дохода в выручке, прибыль; 2) оценить, производство какого изделия наиболее выгодно и наименее выгодно, исходя из приносимого каждым изделием маржинального дохода; 3) рассчитать критический объем производства
- Количественное определение препарата «Kalii bromidum» по фармакопейной статье проводят следующим образом: около 0,2 г препарата (точная масса), предварительно высушенного при 1100С в течение 4 часов, растворяют в 20 мл воды и титруют 0,1 моль/л раствором серебра нитрата до оранжево - желтого окрашивания (индикатор – калия хромат). Калия бромида в высушенном препарате должно быть не менее 99,0 % и не более 100,6 %.
- Рассчитайте коэффициент, при необходимости укрепите или разбавьте 0,1 М раствор аммония роданида, если при установлении титра на 25 мл 0,1 М раствора серебра нитрата израсходовано 26,05; 26,00; 26,00 мл приготовленного раствора роданида аммония. Был приготовлен 1 л раствора, израсходовано на анализ 80 мл.
- Рассчитайте коэффициент, при необходимости укрепите или разбавьте 0,1 М раствора йода. Если при установлении титра на 25 мл раствора тиосульфата натрия (0,1 М) было израсходовано 24,30, 24,40, 24,30 мл 0,1 М раствора йода.
- Рассчитайте коэффициент, при необходимости укрепите или разбавьте 0,1 М раствор калия бромата, если при установлении титра на 25 мл приготовленного раствора израсходовано 25,55; 25,60; 25,65 мл 0,1 М раствора тиосульфата натрия. Был приготовлен 1 л 0,1 М раствора калия бромата, потрачено на анализ 100 мл.
- . Закончите уравнение реакции (в случае если реакция возможна): K2SO3 + HCl = Na2CO3 + H2SO4 = K 2 SO 4 + NaCl = Запишите полное и сокращенное ионные уравнения данных реакций.
- Рассчитайте коэффициент, при необходимости укрепите или разбавьте 0,1 М раствор хлористоводородной кислоты, если при установлении титра на 0,1543 г натрия карбоната было израсходовано 30 мл приготовленного раствора хлористоводородной кислоты, на 0,1539 г 29,95 мл, на 0,1594 г 31,05 мл. Был приготовлен 1 л 0,1 М раствора хлористоводородной кислоты, израсходовано на анализ 170 мл.
- Рассчитайте фактор реакции, молярную массу эквивалента, титр титранта по определяемому веществу при количественном определении калия йодида (М.м. 166,01) методом Фаянса (титрант 0,1 моль/л раствора серебра нитрата). Дайте обоснование данному методу количественного определения.
