
Запишите уравнение реакции Вашего варианта (табл.1). 1) Определите эквиваленты и эквивалентные массы исходных веществ; (Решение → 25932)
Заказ №38836
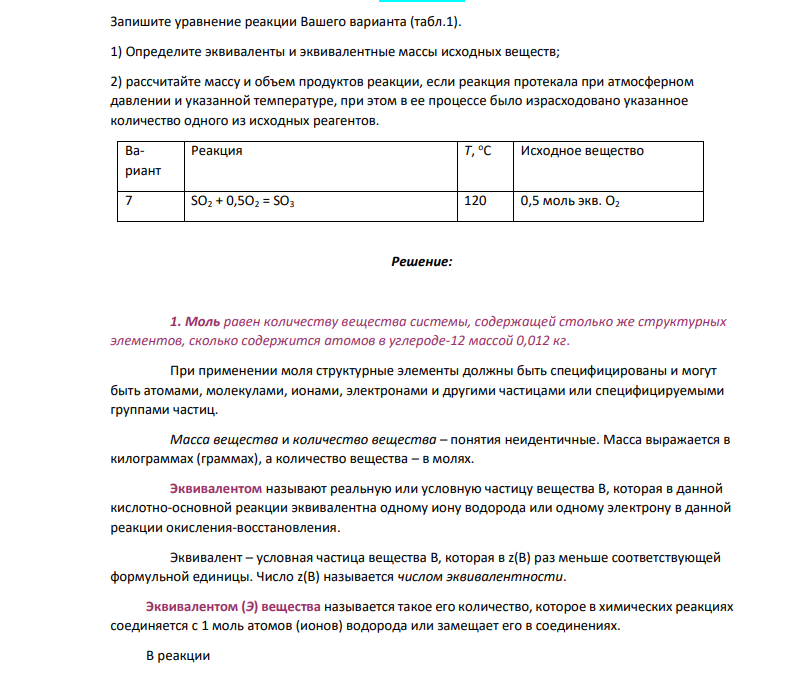
Запишите уравнение реакции Вашего варианта (табл.1). 1) Определите эквиваленты и эквивалентные массы исходных веществ; 2) рассчитайте массу и объем продуктов реакции, если реакция протекала при атмосферном давлении и указанной температуре, при этом в ее процессе было израсходовано указанное количество одного из исходных реагентов. Вариант Реакция Т, оС Исходное вещество 7 SO2 + 0,5O2 = SO3 120 0,5 моль экв. O2
Решение:
1. Моль равен количеству вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 0,012 кг. При применении моля структурные элементы должны быть специфицированы и могут быть атомами, молекулами, ионами, электронами и другими частицами или специфицируемыми группами частиц. Масса вещества и количество вещества – понятия неидентичные. Масса выражается в килограммах (граммах), а количество вещества – в молях. Эквивалентом называют реальную или условную частицу вещества В, которая в данной кислотно-основной реакции эквивалентна одному иону водорода или одному электрону в данной реакции окисления-восстановления. Эквивалент – условная частица вещества В, которая в z(В) раз меньше соответствующей формульной единицы. Число z(В) называется числом эквивалентности. Эквивалентом (Э) вещества называется такое его количество, которое в химических реакциях соединяется с 1 моль атомов (ионов) водорода или замещает его в соединениях. В реакции SO2 + 0,5O2 = SO3 Из уравнения реакции видно, что для образования триоксида серы необходимо 1 моль диоксида серы и 0,5 моль кислорода. Следовательно, 1 моль ионов водорода соответствует 1 моль диокисда серы SO2 и 0,5 моль O2, поэтому Э (SO2) = 1 моль, Э (O2) = 0,5 моль. Масса 1 эквивалента вещества (элемента) называется его молярной массой эквивалента (М(1/z, В)). Таким образом, эквиваленты выражаются в молях, а молярные массы эквивалентов – в г/моль. Поэтому Мэкв (SO2) = 48/4=12 г/моль; Мэкв (O2) = 0,5*32/4=4 г/моль. 2. По закону эквивалентов количество моль эквивалентов диоксида серы равно количеству моль эквивалентов кислорода, т.е. nэкв (SO3) = nэкв(О2) Согласно условию


- 3. В чем сущность кулонометрического титрования? Какие типы химических реакций можно использовать в кулонометрическом титровании?
- Необходимо рассчитать показатель ЧДД для оценки: - потенциальной эффективности проекта; - общей коммерческой эффективности проекта; - эффективности участия предприятия в инновационном проекте. Денежные потоки инновационного проекта приведены в таблице 2. Шаг расчета равен одному году, постоянная во времени норма дисконта равна 15%. Кредитный процент 14 % годовых Депозитный процент составляет 15% годовых для средств, вкладываемых с целью обеспечения финансовой реализуемости проекта.
- 2. Объясните необходимость использования фонового электролита при проведении вольтамперометрических измерений. Каким требованиям должен удовлетворять фоновый электролит?
- В чем разница между понятиями первичные спирты, вторичные спирты и третичные спирты? Приведите схемы и назовите продукты реакций бутилового и втор-бутилового спиртов со следующими реагентами: a) SOCl2; б) Cu (300°С); в) КМnО4 (Н+ ).
- Описать методы количественного определения, применяемый в фармацевтическом анализе. Характеристику каждого метода проводить на конкретных примерах с уравнениями реакций, расчетом факторов эквивалентности; отметить достоинства и недостатки данного метода
- 1. Какие индикаторные электроды можно использовать при потенциометрическом титровании смеси соляной и уксусной кислот раствором щелочи? Какой вид будет иметь кривая титрования? Как рассчитать содержание каждой кислоты?
- Золь иодида серебра, получаемый по реакции: KI+AgNO3→AgI+KNO3 при некотором избытке KI , коагулируют растворами сульфата калия и ацетата кальция. Коагулирующее действие какого электролита сильнее?
- 6. Укажите последовательность проведения количественного флуориметрического анализа методом градуировочного графика. Что называют квантовым выходом?
- Приведите свой пример таблицы погашения кредита дифференцированными и аннуитетными платежами
- 5. Чему равна концентрация никотина в экстракте из листьев табака в мг/100г, если интенсивность люминесценции пробы составляла 0,24, а значения величин люминесценции стандартных растворов приведены в таблице?
- 4. Рассчитайте Сэкв(Na2SO4), если при амперометрическом титровании 10,00 см3 раствора сульфата натрия раствором ацетата свинца, Сэкв ((CH3COO)2Pb) = 0,0350 моль/дм3 , получены следующие данные:
- Инновационный проект потребует для своего осуществления 5 лет и затрат капитала 365 млн. р., которые необходимо инвестировать сразу же, и ещё 135 млн. р. в следующем году.
- Напишите схемы реакций получения бутилацетата из этанола и фенилацетата из фенола. Укажите на различия в способах получения сложных эфиров из спиртов и фенолов.
- Рассчитайте, какую навеску порошка растертых таблеток кислоты аскорбиновой следует взять для количественного определения, чтобы на титрование израсходовалось 10,00 мл раствора калия йодата с К 1,0000. Таблетки по 0,05г, средняя масса таблеток 0,200 г.
