
Дано уравнение реакции (см. вариант в табл. 4). 1. Для всех веществ, участвующих в реакции, выпишите из приложения 1 значения стандартных термодинамических величин (Решение → 44580)
Заказ №70603
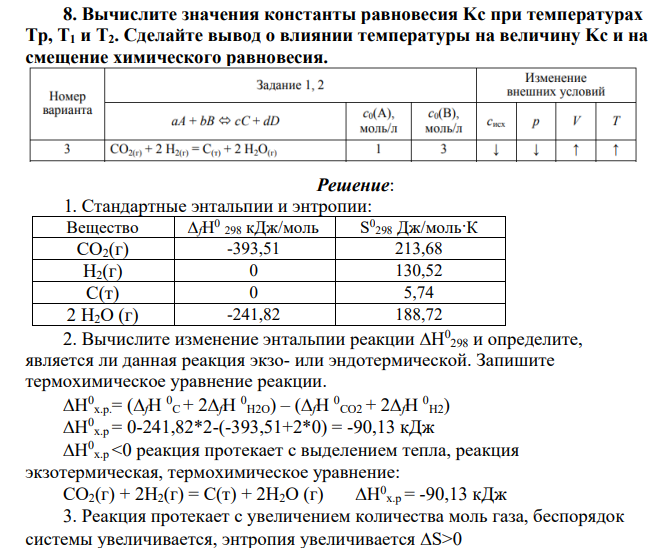
Дано уравнение реакции (см. вариант в табл. 4). 1. Для всех веществ, участвующих в реакции, выпишите из приложения 1 значения стандартных термодинамических величин Hf 0 298 и S0 298 . 2. Вычислите изменение энтальпии реакции H0 298 и определите, является ли данная реакция экзо- или эндотермической. Запишите термохимическое уравнение реакции. 3. По виду уравнения реакции, не прибегая к расчетам, определите знак изменения энтропии реакции S 0 298 . Вычислив изменение энтропии реакции в стандартных условиях, объясните знак S 0 298. 4. Вычислите энергию Гиббса прямой реакции в стандартных условиях 0 G0 298 и установите возможность самопроизвольного протекания реакции. 5. Определите температуру, при которой реакция находится в равновесии (Тр). 6. Рассчитайте G при Т1 = Тр–100, Т2 = Тр+100. 7. Постройте график зависимости G от Т и обозначьте на графике область температур самопроизвольного протекания реакции. 9 8. Вычислите значения константы равновесия Kc при температурах Тр, Т1 и Т2. Cделайте вывод о влиянии температуры на величину Kc и на смещение химического равновесия.
Решение:
1. Стандартные энтальпии и энтропии: Вещество ∆fН0 298 кДж/моль S 0 298 Дж/моль·К CO2(г) -393,51 213,68 Н2(г) 0 130,52 C(т) 0 5,74 2 Н2О (г) -241,82 188,72 2. Вычислите изменение энтальпии реакции H0 298 и определите, является ли данная реакция экзо- или эндотермической. Запишите термохимическое уравнение реакции. 0 х.р.= (f 0 C + 2f 0 H2O) – (f 0 CO2 + 2f 0 H2) 0 х.р = 0-241,82*2-(-393,51+2*0) = -90,13 кДж 0 х.р <0 реакция протекает с выделением тепла, реакция экзотермическая, термохимическое уравнение: CO2(г) + 2H2(г) = C(т) + 2Н2О (г) 0 х.р = -90,13 кДж


- Предприятие получило в банке ссуду в размере 10 млн.р. сроком на 4 года на следующих условиях: процентная ставка в первый год – 25% годовых; для второго года
- Получен кредит в сумме 4 млн.р. сроком на 3 года. По договору процентная ставка для первого года – 25% годовых, в последующие годы установлена маржа в размере 3%. Какую сумму
- Изобразить все возможные таутомерные формы Dарабинозы, назвать их
- Получить масляную кислоту из соответствующего спирта. Написать схемы реакций взаимодействия этой кислоты: а) с гидроксидом калия; б) карбонатом натрия; в) метанолом
- Написать уравнение реакции 3-метилбутанола-2 с: а) уксусной кислотой; б) PCl5; в) бромистым водородом
- Стирол, строение. Написать для него реакции с: а) хлором; б) гидрирования; в) полимеризации
- Написать формулы пяти кислот, которые обычно входят в состав жиров и масел. От чего зависит консистенция жиров? Привести каталитическое гидрирование стеаринодиолеата глицерина
- Какой объем 2 М раствора NH4OH теоретически необходим для осаждения Al(OH)3 из 200 мл 30 %-го раствора хлорида алюминия, плотность которого 1,3 г/мл
- Показать схемами диссоциации и уравнениями реакций, как изменяются свойства гидроксидов в ряду В(ОН)3 – Аl(ОН)3 – Gа(ОН)3 – Тl(ОН)3. Объяснить наблюдаемую закономерность
- Используя значения fGº298 газообразных СF4, CCl4, CBr4, CI4, соответственно равные –888; –60,6; 66,9 и 260,9 кДж/моль, сравнить устойчивость тетрагалогенидов углерода, и оценить возможность
- Какое соединение более гидролизуется в водном растворе: SnCl2 или SnCl4? В каком растворе при одинаковой молярной концентрации больше pH? Какое соединение образует SnCl4 c продуктом гидролиза
- Объем валовой продукции на предприятии – 2000 штук в год. Затраты на сырье составляют 82 руб. на единицу продукции или 70% от ее производственной себестоимости. Затраты на реализацию продукции и прочие
- Предприятие реализовало продукцию на 220 млн.руб. за год. Оборачиваемость оборотных средств составила 14 дней. Рассчитайте изменение коэффициента оборачиваемости и сумму
- Постройте и прокомментируйте график. Избыток спроса или предложения наблюдается на рынке при цене 30 у.е.? Объем тыс.шт. Цена
