
Цель работы: определение теплового эффекта системы, в которой происходит химическая реакция, и энтальпии реакции в нестандартных условиях (Решение → 35684)
Заказ №38744
Цель работы: определение теплового эффекта системы, в которой происходит химическая реакция, и энтальпии реакции в нестандартных условиях
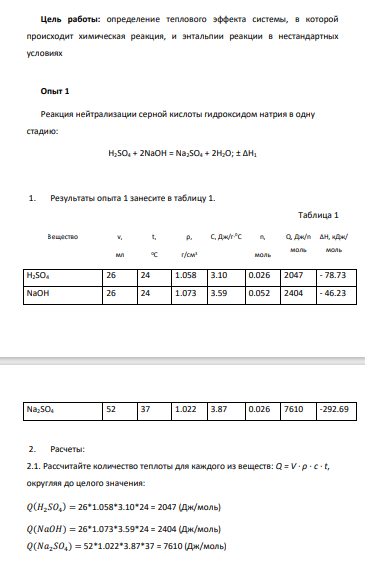
Опыт 1 Реакция нейтрализации серной кислоты гидроксидом натрия в одну стадию: H2SO4 + 2NaOH = Na2SO4 + 2H2O; ± ∆Н1 1. Результаты опыта 1 занесите в таблицу 1.
Таблица 1 Вещество v, мл t, 0С ρ, г/см3 С, Дж/г∙0С n, моль Q, Дж/n моль ∆Н, кДж/ моль H2SO4 26 24 1.058 3.10 0.026 2047 - 78.73 NaOH 26 24 1.073 3.59 0.052 2404 - 46.23 Na2SO4 52 37 1.022 3.87 0.026 7610 -292.69 2. Расчеты: 2.1. Рассчитайте количество теплоты для каждого из веществ: Q = V · ρ · c · t, округляя до целого значения: 𝑄(𝐻2𝑆𝑂4 ) = 26*1.058*3.10*24 = 2047 (Дж/моль) 𝑄(𝑁𝑎𝑂𝐻) = 26*1.073*3.59*24 = 2404 (Дж/моль) 𝑄(𝑁𝑎2𝑆𝑂4 ) = 52*1.022*3.87*37 = 7610 (Дж/моль)

- Во время отдыха на курорте из гостиничного номера Сергеевой в её отсутствие была похищена фамильная ценность девушки, янтарный кулон. Гостиница возместила стоимость похищенной вещи, но найти похитителя так и не удалось.
- Для определения концентрации раствора арсенита натрия взяли 0,1182 г стандартного образца стали, с массовой долей марганца 0,84%.
- В 2002 году по сравнению с 2001 годом на потребительском рынке Тюменской области общее изменение потребительских цен составило +16%
- Предположим, что инвестиции составляют 400 млрд. р. Норма чистой прибыли, скорректированная на уровень инфляции, составляет 8 %.
- Одно железное изделие покрыли никелем, другое – оловом. Обосновать, к какому типу относятся покрытия.
- Кинетические измерения показали, что реакция 2 2 2NO O 2NO имеет третий порядок. В начальный момент концентрации исходных веществ равны 0 NO и 2 0 O .
- Вычислите молярные массы эквивалентов и эквиваленты Р2О5 в реакциях, идущих по уравнениям: Р2О5 + 3MgO = Mg3(PO4)2; (1) P2O5 + MgO = Mg(PO3)2. (2)
- Гражданка РФ и гражданин Судана, оба исповедующие ислам, хотели заключить брак в органах ЗАГСа, но им было отказано, поскольку гражданин Судана уже имеет другой зарегистрированный брак. С целью заключения брака, в результате которого гражданка РФ становится второй женой, они переехали в Судан, где брак был заключен
- Каким образом можно оценить качество окружающей среды? Качество окружающей среды — это степень соответствия природных условий физиологическим возможностям человека.
- Ниже приведены данные об уровнях производства и затратах за период: Объем производства, тыс. шт. 0 1 2 3 4 5 Общие затраты, тыс. руб. 800 1200 1600 2000 2400 2800
- По условным схемам напишите уравненияя аналитической реакции: - берлинская лазурь; как препарат кальц
- Сколько моль эквивалентов металла вступило в реакцию с кислотой, если при этом выделилось 5,6 л водорода при нормальных условиях?
- Напишите электронные формулы атомов элементов с зарядом ядра: а)+46, 6) +105; в) +114 и в) еще не открытого элемента с зарядом ядра +120. К каким электронным семействам относятся эти элементы?
- По значениям констант скоростей реакции 2 2 2HI H I при двух температурах (табл.4) определите: 1) температурный коэффициент скорости реакции (по правилу Вант-Гоффа); 2) энергию активации Е; 3)константу скорости 3 k при температуре Т3; 4) число общих столкновений в 1 л за 1 с (предэкспотенциальный множитель k0 в уравнении Аррениуса) при Т3; 5) долю активных столкновений /( ) E RT e при Т3; 6) сделать вывод из сопоставления общих и активных столкновений. Таблица 5 Зависимость константы скорости от температуры Вариант Т1, К k1,л/(моль∙с) Т2, К k2,л/(моль∙с) Т3, К 14 575 1,22∙10-6 647 8,59∙10-5 610
