
Для обратимой химической реакции A (см.таблицу 1.III.2.12) определите: а) изменение энергии Гиббса G°T при стандартном давлении и температуре T; б) константу равновесия реакции A при заданной температуреT; (Решение → 26306)
Заказ №38753
Задание 1.6. Для обратимой химической реакции A (см.таблицу 1.III.2.12) определите: а) изменение энергии Гиббса G°T при стандартном давлении и температуре T; б) константу равновесия реакции A при заданной температуреT; в) изменение энергии Гиббса GT при температуре T и парциальных (неравновесных) давлениях реагентов равных PB, PС, PD и PE (см. таблицу 1.III.2.12). На основании расчетов сделайте заключение о направлении протекания самопроизвольного процесса в заданных условиях. Выразите в общем виде взаимосвязь между константы равновесия и химической переменной (глубиной превращения) реакции, полагая, что все участники реакции взяты в стехиометрических количествах и находятся в идеальном газообразном состоянии. Проанализируйте, как повлияет на равновесный выход продукта D: а) увеличение (в изотермических условиях, т.е. при T = const) общего давления в системе; б) разбавление реакционной смеси инертным газом в изобарноизотермических условиях.
Решение:
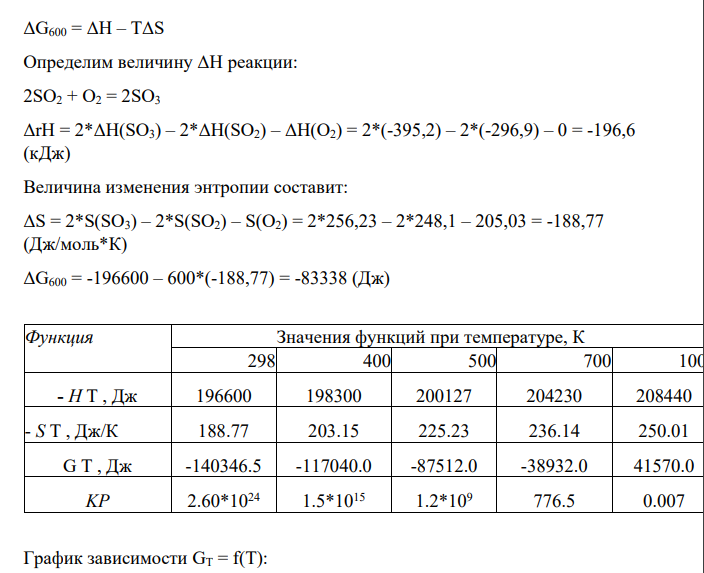
При температуре T = 600 К изменение энергии Гиббса в ходе реакции синтеза метанола будет равно: 215 220 225 230 235 240 245 250 200 400 600 800 1000 1200 - Sт, Дж/моль*К T, K ΔG600 = ΔH – TΔS Определим величину ΔН реакции: 2SO2 + O2 = 2SO3 ΔrН = 2*ΔH(SO3) – 2*ΔH(SO2) – ΔH(O2) = 2*(-395,2) – 2*(-296,9) – 0 = -196,6 (кДж) Величина изменения энтропии составит: ΔS = 2*S(SO3) – 2*S(SO2) – S(O2) = 2*256,23 – 2*248,1 – 205,03 = -188,77 (Дж/моль*К) ΔG600 = -196600 – 600*(-188,77) = -83338 (Дж) Функция Значения функций при температуре, К 298 400 500 700 100- Н T , Дж 196600 198300 200127 204230 208440 - S T , Дж/К 188.77 203.15 225.23 236.14 250.01 G T , Дж -140346.5 -117040.0 -87512.0 -38932.0 41570.0 KP 2.60*1024 1.5*1015 1.2*109 776.5 0.007 График зависимости GT = f(T):


- Определите изменение энтропии в результате протекания химической реакции A (см. таблицу 1.III.2.1) в стандартных условиях и при температуреT (все вещества, участвующие в реакции находятся в идеальном газообразном состоянии). Для выполнения задания воспользуйтесь уравнениемСP =f(T), составленном при выполнении задания 1.2. Постройте график зависимости ΔST =f(T)
- Определите абсолютную энтропию вещества B (см.таблицу 1.III.2.7) при заданных температуре T2 > 298К и давлении P2` < 1013220 Па на основании справочных данных для стандартного значения энтропии S°298 и истинной изобарной теплоемкости.
- Годовой объем добычи нефти составил 1600 тыс. тонн, газа 580 млн. м 3 , газового конденсата 750 тыс. тонн. Плотность газа в поверхностных условиях равна 0,707 кг/м3 (теплота сгорания добытого газа соответствует теплоте сгорания условного газа).
- Эффективный фонд времени работы одного рабочего в год – 1800 час. Коэффициент выполнения норм – 1,2. Численность вспомогательных рабочих в цехе составляет 25 % от численности основных рабочих. Плановый процент невыходов на работу составляет 10%. З
- По данным табл. 2 определить среднегодовую, среднедневную, среднечасовую выработку на 1 работника; среднемесячную заработную плату; абсолютный прирост этих показателей в отчетном году.
- При какой температуре наступит равновесие системы 4НСl(г) + О2(г) = 2Н2О(г) + 2Сl2(г); Н = –114,2 кДж? Что в этой системе является более сильным окислителем: хлор или кислород?
- Определить сумму амортизации по годам линейным способом, методом уменьшаемого остатка, методом по сумме чисел лет для станка стоимостью Сп (по вариантам) со сроком полезного использования СПИ – 5 лет.
- Теория растворов сильных и слабых электролитов Определите ионную силу водного раствора электролита А (табл. 3.1), если: а) моляльная концентрация электролита А в растворе равнаm; б) моляльная концентрация электролита А в растворе равна m и в растворе присутствует электролит В с концентрацией m1;
- Определите парциальное давление вещества С при давлении Р и стехиометрическом соотношении начальных веществ реакции В (см.таблицу 1.III.2.20). Для расчетов воспользуйтесь значениями средней изобарной теплоемкости реагентов.
- Полная балансовая стоимость основных средств (фондов) нефтегазодобывающего предприятия на начало отчетного года составила 212 млрд. руб. Их структура (в % к балансовой стоимости) представлена в табл.4. Полная балансовая стоимость основных средств (фондов) нефтегазодобывающего предприятия на начало отчетного года составила 212 млрд. руб.
- Используя справочные данные для температурной зависимости истинной теплоемкости СP =f(T) веществ, участвующих в химической реакции A, составьте уравнения температурных зависимостей теплового эффекта HT =f(T), константы равновесия lnKP,T =f(T) и убедитесь в их правильности.
- Каковы темпы роста степени вертикальной интеграции нефтяной компании за год? Исходные данные приведены в табл.3.
- Для химической реакцииA (см.таблицу) определите степень превращения веществB (D),C (E) и определите состав равновесной газовой смеси (мол.%) при температуреT и атмосферном давлении, если исходные вещества были взяты в количествах nо,CO = nо,H2 = 2 моль.
- По данным табл.1 Добыча нефти 400 тыс.т определить базисные и цепные темпы роста и темпы прироста объемов валовой продукции по видам и по предприятию в целом (в натуральном и стоимостном выражении) за анализируемый период. Выявить влияние цен на изменение объемов производства.
