
Ирина Эланс
Из анализируемого раствора, содержащего ионы металла М3+, в результате электролиза при силе тока 1 А за 50 мин было выделено на катоде 0,2800 г металла. Определить, какой металл выделился на катоде. (Решение → 12287)
Заказ №38777
3. Из анализируемого раствора, содержащего ионы металла М3+, в результате электролиза при силе тока 1 А за 50 мин было выделено на катоде 0,2800 г металла. Определить, какой металл выделился на катоде.
Решение:
При электролизе на катоде происходит восстановление катионов металла:
Катод (−): M3+ + 3e − → М
Масса металла (m, г), выделившегося при электролизе, определяется по закону Фарадея:
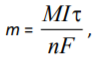


- Задача Провести анализ возрастного состава оборудования по количеству и структуре, оценить возрастной состав оборудования. Провести сравнение со средним возрастом: по каждому виду оборудования, по всем его видам по итоговым данным. Видоборудования до 5 лет от 5 до 10 лет Металлорежущее Кузнечнопрессовое Подъёмно- транспортное Энергетическое Итого шт. 50 Срок эксплуатации в годах шт. 60 30 26 80 от 10 до свыше 20 20 лет лет шт. шт. 20 16 90
- При анализе сурьмяного блеска Sb2S3 была взята навеска в 0,1872 г. После соответствующей обработки вся сера была переведена в SO4 2- , который определили в виде BaSO4, причем вес последнего оказался равным 0,3243 г. Вычислите процентное содержание Sb2S3, в анализируемой пробе сурьмяного блеска.
- Условие практического задания: на основании приведённых данных определить средний коэффициент сортности по плану и фактически и индекс роста качества продукции. Сорт продукции Цена, руб. 5500 3330 1400 план 2100 1640 1500 Выпуск продукции, шт. факт 3300 1550
- План сбыта продукции на год содержит следующие данные. План сбыта продукции на год: Отчет предыдущего года Планируемый год Продукция объем объем продаж, тыс. цена, руб. продаж, тыс. цена, руб.
- Потенциальный ВВП, на уровне которого изначально находится экономика, равен 2000 млрд. руб. Кривая краткосрочного совокупного предложения (SRAS) горизонтальна.
- На основании приведенных данных проанализируйте влияние факторов на изменение прибыли и рентабельности отдельных видов продукции и в целом по предприятию: Изделие А Изделие В Показатель Прошлый Отчетный Прошлый Отчетный 1. Объем производства, шт. 2. Цена изделия, тыс.
- В чем состоит сущность гравиметрического анализа? Как рассчитывается результат анализа в гравиметрии? Ответ: Гравиметрия (весовой анализ) — метод количественного анализа в аналитической химии, который основан на измерении массы определяемого компонента, выделенном в виде веществ определённого состава.
- Текущий курс евро к рублю составляет 32,0 руб. /евро. На валютной бирже представлена следующая структура заявок на покупку и продажу: На продажу На покупку Курс, не менее, Объем, млн. евро Курс, не более, Объем, млн. евро руб./евро руб. /евро 31,0 31,0 2,1 31,2 9,6 31.4 9,1 31.4 5,2
- Чему равна плотность по водороду сжатого газа, имеющего следующий объемный состав: 32% СН4; 5% N2; СО2; 4% С2Н4; 9% СО.
- Вычислить массу и количество молей водяного пара в закрытом помещении коровника объемом 10 000 м3 , если парциальное давление этого пара 1200 Па, а температура воздуха 10оС. Дано: Н2О V=10 000 м3 t=10оС р=1200 Па Найти: m, v
- Предприятие при продаже товара оказывает скидки постоянным клиентам в размере 5%. Провести анализ скидок и рассчитать, какой объем продаж необходимо выполнить для сохранения соответствующего уровня маржинального дохода?
- Проанализируйте данные зависимости успеваемости (балл в сессию) магистрантов группы ЭКмз-1501 в весеннюю сессию 2015-2016 учебного года по курсу «Статистика» от пропущенных ими занятий во 2-ом семестре (
- Главный инженер предприятия отработал в текущем месяце 24 дня из 28 рабочих дней. На четыре дня он брал отпуск за свой счет по семейным обстоятельствам. Оклад работника за полный рабочий месяц составляет 36 000 рублей. Работник имеет двух несовершеннолетних
- . Приготовление и стандартизация раствора иода (I2). Укажите свойства раствора, и условия его хранения. Напишите уравнения реакций и выведите формулу для расчета нормальной концентрации иода (fэкв = 1/2) по результатам титрования.
