
Какие из перечисленных ниже веществ взаимодействуют с перманганатом калия в кислотной среде: оксид свинца (IV), пероксид натрия, хлороводородная кислота, сульфат железа (II), сульфат железа (III), нитрат серебра. (Решение → 34729)
Заказ №38812
Какие из перечисленных ниже веществ взаимодействуют с перманганатом калия в кислотной среде: оксид свинца (IV), пероксид натрия, хлороводородная кислота, сульфат железа (II), сульфат железа (III), нитрат серебра. Составьте уравнения протекающих реакций.
Решение:
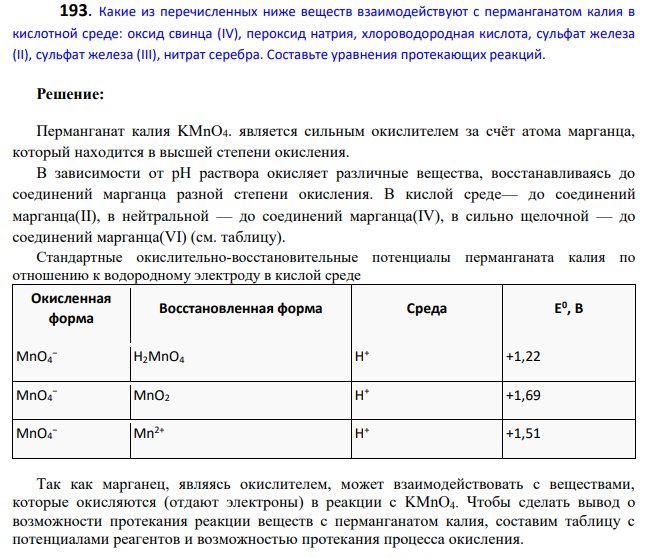
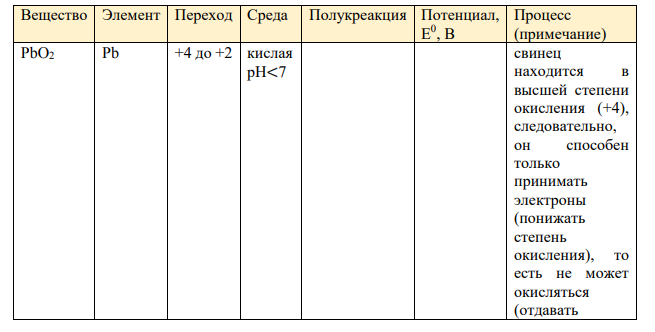
Перманганат калия KMnO4. является сильным окислителем за счёт атома марганца, который находится в высшей степени окисления. В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде— до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI) (см. таблицу). Стандартные окислительно-восстановительные потенциалы перманганата калия по отношению к водородному электроду в кислой среде Так как марганец, являясь окислителем, может взаимодействовать с веществами, которые окисляются (отдают электроны) в реакции с KMnO4. Чтобы сделать вывод о возможности протекания реакции веществ с перманганатом калия, составим таблицу с потенциалами реагентов и возможностью протекания процесса окисления. Вещество Элемент Переход Среда Полукреакция Потенциал, Е 0 , В Процесс (примечание) PbO2 Pb +4 до +2 кислая рН<7 свинец находится в высшей степени окисления (+4), следовательно, он способен только принимать электроны (понижать степень окисления), то есть не может окисляться (отдавать Окисленная форма Восстановленная форма Среда E 0 , В MnO4 − H2MnO4 H + +1,22 MnO4 − MnO2 H + +1,69 MnO4 − Mn2+ H + +1,51


- Ставка простых процентов по кредиту определена следующим образом: первые три месяца ставка составляет 12% годовых. Следующие девять месяцев ставка увеличивается на 1,2% и на последующий период ставка составляет 14%. Общий срок кредита в размере 120 тыс. руб. составляет два с половиной года. Определите наращенную сумму и сумму начисленных процентов
- Номинальный ВВП в 2004г. (базисном) составил 400 млрд. долл., а в 2005 г. – 440 млрд. долл. Индекс-дефлятор ВВП в 2005 г. был равен 125%. Как изменился реальный ВВП 2005 г. по сравнению с реальным ВВП 2004г.?
- Во сколько раз уменьшится свободная поверхностная энергия водяного тумана, если при этом радиус его капель увеличится от 1 мкм до 1,2 мм.
- Суда 250 тыс. руб. выдана на семнадцать месяцев по номинальной ставке 12% годовых. Начисление процентов производится по полугодиям. Определите наращенную сумму при её вычислении смешанным способом.
- Для указанного водного раствора (таблица 1) при температуре 20°С и давлении 101325 Па определить:
- В течение года предприятием реализовано продукции на сумму 510 000 тыс. руб., располагая оборотными средствами в размере 70 000 тыс. руб.
- За 2008 г. производительность труда при посадке цветочных растений в горшки составляет 120% при средней норме выработки 960 горшков на 1чел/день, в 2009 г. – 110%, а норма выработки благодаря совершенствования технологии работ были увеличены на15%.
- Для определения содержания сульфат-ионов в воде минерального источника к 150,0 мл её прибавили 25,00 мл 0,01115 М BaCl2. Не фильтруя осадок BaSO4, добавили к смеси аммонийный буфер, содержащий комплексонат магния.
- Для соединений варианта -укажите структурную формулу и характерные фрагменты строения, укажите наличие первичных вторичных, третичных четвертичных атомов углерода; - приведите все возможные названия вещества;
- Кредит в размере Р = 54 000 руб. выдается на п + 0,5 = 6 + 0,5 = 6,5 года. Ставка процентов за 1-й год – 5%, а за каждое последующие полугодие она увеличивается на 1,5%. Определить коэффициент наращения и наращенную сумму.
- Оприделить современную величину суммы 150 00 руб., которая будет выплачена через три года и девять месяцев при помесячном начислении сложных процентов по ставке 8 % годовых. Используйте смешанный способ расчетов.
- Вычислить массовую долю (%) меди в руде, если из навески руды массой 0,6215 г медь перевели в раствор в виде Cu2+ и после добавления к этому раствору KI выделившийся йод оттитровали 18,23 мл раствора тиосульфата натрия с T(Na2S2O3) = 0,01545.
- Определение направления процесса по уравнению изотермы химической реакции
- На основании стандартных теплот образования н абсолютных стандартных энтропий соответствующих веществ, вычислите ΔG 0 реакции протекающей по уравнению:
