
Ирина Эланс
Составьте схему электролиза расплава и водного раствора солей FeCI3 и Ba(NO2)2 на инертных электродах. Определите объем газа (187С, 233 мм.рт.ст.) и массу металла, выделившихся на электродах при электролизе 69,8 г расплава Ba(NO2)2. (Решение → 21943)
Заказ №39035
Составьте схему электролиза расплава и водного раствора солей FeCI3 и Ba(NO2)2 на инертных электродах. Определите объем газа (187С, 233 мм.рт.ст.) и массу металла, выделившихся на электродах при электролизе 69,8 г расплава Ba(NO2)2.
Решение: Раствор FeCl3 FeCl3 Fe3+ + 3ClНа аноде: 2Cl- - 2e = Cl2 На катоде: Fe3+ + 3e = Fe Суммарная реакция: 2FeCl3 электролиз 3Cl2 + 2Fe Расплав FeCl3 На аноде: 2Cl- - 2e = Cl2 На катоде: Fe3+ + 3e = Fe Суммарная реакция: 2FeCl3 электролиз 3Cl2 + 2Fe Раствор Ba(NO2)2 На аноде: 2Н2O - - 4e = O2 + 4H+

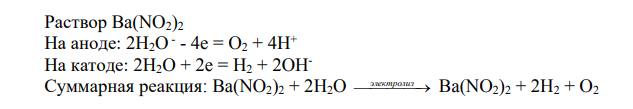

- Анализ вещества, состоящего из углерода, водорода и хлора, дал следующие результаты: С – 42,6%, Н – 7,1%, Cl – 50,3%. Определите
- Конкурентный рынок характеризуется функцией предложения Qs=3P-2 и функцией спроса QD=40-3P. Правительство вводит потоварный налог на продукцию производителей в размере 2
- 2.43. Определите период обращения Т искусственного спутника, вращающегося по круговой орбите радиусом R = 42106 м. Радиус Земли равен R0 = 6,4106 м, ускорение свободного падения на поверхности Земли равно g0 = 9,8 м/с2 Дано: R = 42106 R0 = 6,4106 g0 = 9,8 м/с2 Найти: Т
- Рассчитать pH 0,2 м раствора лимонной кислоты (Ка = 7,4*10-4 ).
- По данным анализа вещество содержит 85,7% С и 14,3% Н. Определение молекулярной массы дало значение 723. Какова молекулярная формула вещества
- Компания А получает выручку в размере 1400 тыс.руб. в год. Себестоимость реализованной продукции 1250 тыс.руб. Ставка налога на прибыль 20%. Долг компании привлечен на условиях: долгосрочный - под 14% годовых, краткосрочный – под 12%. Компания выплачивает на дивиденды 40% от чистой прибыли, остальное расходуя на инвестиции, на приобретение основных средств.
- Конкурентный рынок характеризуется функцией предложения Qs=3P-2 и функцией спроса QD=40-3P. Чему равна эластичность предложения по цене в условиях равновесия?
- Отклонение гальванометра однолучевого фотоколориметра при исследовании раствора К2Сr2О7 составляет 75 делений шкалы. После добавления в кювету 1 мл стандартного 0,015 н. раствора бихромата калия при постоянной толщине слоя отклонение составило 65 делений
- В простой традиционной модели монополистической конкуренции фирма имеет функцию издержек LTC=4q+q 2+2. Функция спроса на продукцию фирмы Р=8-q.
- Возможно ли разложение СО2 (г) по уравнению: 2СО2 (Г) = 2СО (г) + О2 (г)
- Рассчитать pH раствора, полученного смешиванием 25 см3 0,25 м серной кислоты и 25 см3 0,30 м раствора гидроксида калия.
- Компания АВС по производству продуктов привлекает долг в среднем под 12% годовых. Безрисковая ставка доходности 6 %. Плата за риск фондового рынка РФ 8 %. Баланс компании А за 2019 г: 1. Внеоборотные активы 500 3. Капитал и резервы 540 2. Оборотные активы 700 4.Долгосрочные обязательства 300 Запасы 300
- Рассчитать концентрацию ОН-групп в 2,3 м растворе анилина (рКb = 9,37)
- Имело ли место общественно-опасное посягательство на Плотников?
