
Определить объем продуктов сгорания, образующихся при сгорании влажного газа с коэффициентом избытка воздуха α = 1,15 (состав газа см. по приложению 1) (Решение → 32963)
Заказ №38834
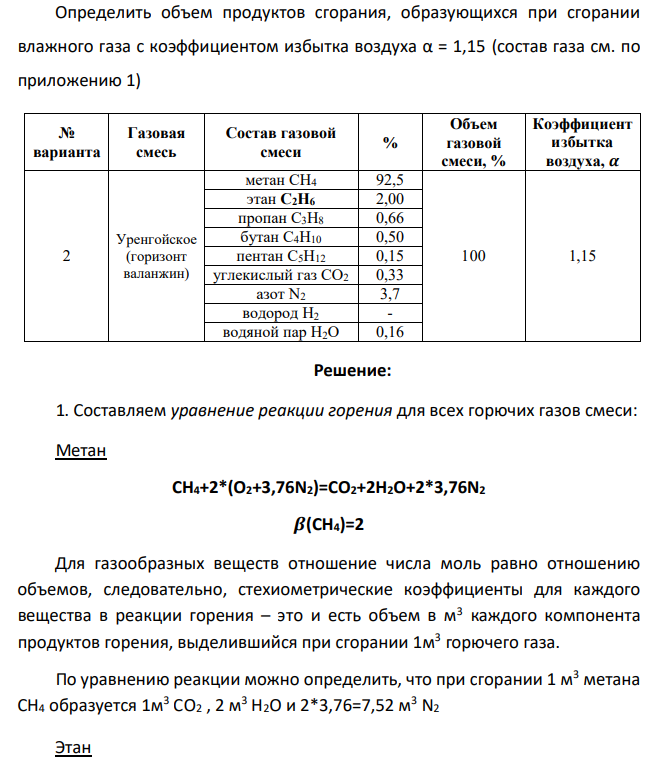
Определить объем продуктов сгорания, образующихся при сгорании влажного газа с коэффициентом избытка воздуха α = 1,15 (состав газа см. по приложению 1) № варианта Газовая смесь Состав газовой смеси % Объем газовой смеси, % Коэффициент избытка воздуха, 𝜶 2 Уренгойское (горизонт валанжин) метан СН4 92,5 100 1,15 этан С2Н6 2,00 пропан C3H8 0,66 бутан C4H10 0,50 пентан C5H12 0,15 углекислый газ СО2 0,33 азот N2 3,7 водород Н2 - водяной пар H2O 0,16
Решение:
1. Составляем уравнение реакции горения для всех горючих газов смеси: Метан CH4+2*(O2+3,76N2)=CO2+2H2O+2*3,76N2 𝜷(CH4)=2 Для газообразных веществ отношение числа моль равно отношению объемов, следовательно, стехиометрические коэффициенты для каждого вещества в реакции горения – это и есть объем в м3 каждого компонента продуктов горения, выделившийся при сгорании 1м3 горючего газа. По уравнению реакции можно определить, что при сгорании 1 м3 метана СН4 образуется 1м3 СО2 , 2 м3 H2O и 2*3,76=7,52 м3 N2 Этан C2H6+3,5*(O2+3,76N2)=2CO2+3H2O+3,5*3,76N2 𝜷(C2H6)=3,5 По уравнению реакции можно определить, что при сгорании 1 м3 этана C2H6 образуется 2м 3 СО2 ,3м 3 H2O и 3,5*3,76=13,16 м 3 N2 560 Пропан C3H8+5*(O2+3,76N2)=3CO2+4H2O+5*3,76N2 𝜷(C3H8)= 5 По уравнению реакции можно определить, что при сгорании 1 м3 пропана C3H8 образуется 3м 3 СО2 ,4м 3 H2O и 5*3,76=18,8 м 3 N2 Бутан C4H10+6,5*(O2+3,76N2)=4CO2+5H2O+3,5*3,76N2 𝜷(C4H10)=6,5 По уравнению реакции можно определить, что при сгорании 1 м3 бутана C4H10 образуется 4м 3 СО2 ,5м 3 H2O и 6,5*3,76=24,44 м 3 N2


- Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДC гальванического элемента, состоящего из свинцовой и магниевой пластин, опущенных в растворы своих солей с концентрацией ионов [Pb2+] = [Mg2+] = 0,01 моль/л. Изменится ли ЭДС этого элемента, если концентрацию каждого из ионов увеличить в одинаковое число раз?
- А.А.Иванов, Б.Б.Петров и В.В.Сидоров обратились с заявлением к администрации Выборгского района Санкт-Петербурга, ООО «Пенёк» о сносе незаконной постройки – здания гипермаркета, возведенного без каких-либо разрешений на территории единственного в районе сквера
- Навеску смеси NaCl и NaNO3 массой 0,8180 г растворили в мерной колбе вместимостью 200 мл. На титрование 20 мл этого раствора израсходовали 18,35 мл раствора 0,0462 M AgNO3.
- Факторный анализ объема валового выпуска продукции за счет использования основных средств Таблица 11 Исходные данные для факторного анализа № п/п Показатель Базисный год Отчетный год Абсолютный прирост Относительный прирост 1 Среднегодовая стоимость основных производственных фондов, тыс. руб
- Азотная кислота плютностью 1,185 г/мл содержит по массе 30,1 % HNO3. Вычислите ее кормальную концептращию в реакции восстановления до NO.
- Определить плотность газа с молекулярной массой 44 г /моль при температуре 150С и избыточном давлении 0,2 МПа.
- На основе данных баланса (табл. 1) предприятия рассчитайте показатели платежеспособности: коэффициент платежеспособности, коэффициент текущей ликвидности, коэффициент обеспеченности собственными средствами, показатели финансовой устойчивости:
- Для о-фурилдиоксимата никеля в хлороформе в, = 1,9х104 л/моль×см. Какое минимальное %-ное содержание Ni в чистом алюминии может быть определено этим реактивом, если масса навески равна 1 г, объем экстракта - 10,0 мл. длина коветы (1) = 5 см. оптическая плотность, при которой погрешность измерения не превышает 10%, равна 0,020?
- Функция общих издержек предприятия имеет вид: ТС = 3000 + 200Q – 2Q2 + 0,01Q3 . Определить алгебраические выражения для FC, VC, ATC, AFC, AVC, MC и построить графики 4-х последних разновидностей издержек при выпуске: Q = 10; 20; … 150.
- В баллоне находится сжиженный газ следующего весового состава: пропан – 65%; бутан -35%. Определить давление в баллоне при температуре 200С.
- Инвестор открыл длинные позиции по акции А и по акции В. Стандартное отклонение доходности акции А за период равно 10%, акции В: 20%. Коэффициент корреляции доходностей равен минус 0,4. Определить риск портфеля за период, если инвестор купил акции А на 75 тыс. руб., акции В на 25 тыс. руб.
- Задание Применение фотометрического анализа в контроле качества многокомпонентных лекарственных средств. Для каждого препарата приведите примеры реакций (напишите уравнения реакций), в результате которых образуются окрашенные соединения:
- Навеска соды (Na2CO3) 1,100 г, содержащая примесь NaCl, растворена и оттитрована 35,0 мл H2SO4 с С1-2.H2804 = 0,500 моль/л. Определите массовую долю Na2CO3 в образце.
- Менеджер управлял портфелем в течение 100 дней. В начале периода в портфель инвестировали 20 млн. руб. Через 100 дней его стоимость выросла до 25 млн. руб. Финансовый год равен 365 дням. Определить доходность управления портфелем в расчете на год: на основе простого процента. на основе эффективного процента
