
При полярографическом определении свинца (II) с применением ртутного капающего электрода навеску анализируемого образца массой 0,7480 г растворили в мерной колбе вместимостью 100 мл, добавили несколько капель раствора желатина и объем раствора довели до метки разбавленной азотной кислотой, используемой в качестве фонового электролита. (Решение → 41103)
Заказ №47045
При полярографическом определении свинца (II) с применением ртутного капающего электрода навеску анализируемого образца массой 0,7480 г растворили в мерной колбе вместимостью 100 мл, добавили несколько капель раствора желатина и объем раствора довели до метки разбавленной азотной кислотой, используемой в качестве фонового электролита. Часть приготовленного раствора перенесли в термостатированную при 25 0С полярографическую ячейку, после продувания раствора током азота (для удаления растворенного кислорода) сняли полярограмму раствора и измерили высоту полярографической волны, равную 142 мм и соответствующую диффузионному току свинца. В аналогичных условиях провели полярографирование стандартного раствора с концентрацией 3,00*10-4 моль/л и получили полярограмму с высотой 118 мм. Рассчитайте массовую долю (%) свинца в анализируемом образце. Напишите уравнение электрохимической реакции, протекающей на ртутном электроде. Нарисуйте схематично полярограмму и покажите, каким образом находят высоту волны графическим способом. Назовите и укажите на рисунке параметр с помощью которого проводят идентификацию вещества полярографическим методом. Объясните, почему в полярографической ячейке поддерживают постоянную температуру раствора, для чего используют фоновый электролит и желатин и почему перед полярографированием раствора из него удаляют кислород.
Решение:
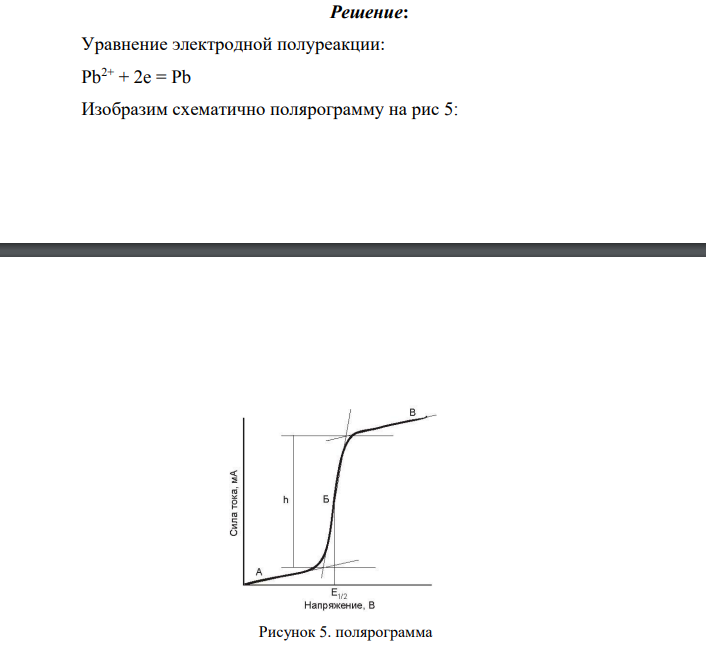
Уравнение электродной полуреакции: Pb2+ + 2e = Pb Изобразим схематично полярограмму на рис 5: Рисунок 5. полярограмма На вольтамперограмме можно выделить три участка. А – пологий участок, ток с изменением потенциала изменяется слабо. Небольшой ток, протекающий на начальном участке вольтамперограммы, называется остаточным, значительную часть которого составляет ток заряжения двойного электрического слоя. Величина остаточного тока имеет порядок ~10−7А (∼0.1 мкА). Б – резкий подъём тока за счет электрохимической реакции (диффузионный ток). При увеличении потенциала достигается потенциал, при котором начинается электрохимическая реакция, то есть электроактивное вещество (деполяризатор) начинает разряжаться на поверхности электрода Сила тока возрастает, на поляризационной кривой наблюдается резкий подъём, электрод деполяризуется. Концентрация ионов-деполяризаторов (восстанавливающихся или окисляющихся ионов) вокруг электрода резко падает, создается обедненный слой, который пополняется ионами за счет процессов механической конвекции и диффузии. Создаются условия, характерные для стационарной диффузии, поэтому ток называется диффузионным 𝐼𝑑.



- В стандартных растворах соли калия с концентрацией с K + были Кизмерены электродные потенциалы калийселективного электрода относительно хлорсеребряного электрода и получены следующие данные с K + , моль/л 0,1 0,01 0,001 0,0001 Е, мВ 100 46 -7 -60
- Навеску диоксида кремния массой м(г) разложили фтороводородной кислотой. Добавили раствор родамина 6Ж и бензола. Интенсивность флуоресценции экстракта по отношению к раствору холостого опыта, проведённому в тех же условиях (Ix-Io).
- Навеску Na2HPO4*12H2O массой 0,5046 г растворили в хлорной кислоте и разбавили до 1000,0 мл. Для построения градуировочного графика в мерные колбы вместимостью 50,0 мл поместили 10,0; 20,0; 25,0; 30,0; 35,0 мл этого раствора, добавили смесь молибдата и метаванадата аммония и разбавили водой до метки.
- Для приготовления стандартного раствора циркония навеску ZrOCl2*8Н2О массой 0,3533 г растворили в 100,0 мл хлороводородной кислоты. В мерные колбы вместимостью 50,0 мл поместили 1,00; 1,20; 1,50; 1,70; 2,00 мл стандартного раствора, прибавили галлоцианин МС (цирконин) и довели до метки водой. Измерили оптические плотности относительно первого раствора.
- Депрессия мочи равна 0.186˚С. Найти осмотическое давление при температуре 36.6˚С.
- Что такое давление насыщенного пара, от чего и как зависит его величина? Уравнение первого закона Рауля.
- Определите знак заряда молекул желатины в растворе с рН = 4,0, если рНиэт = 4,7. К какому электроду будет передвигаться молекула желатины при электрофорезе?
- Тепловой эффект какой реакции равен теплоте образования гидроксида кальция? Вычислите теплоту образования гидроксида кальция, исходя из следующих термохимических уравнений: Са(к) + 1 /2О2(г) = СаО(к); Н = –635,60 кДж; (1) Н2(г)+ 1 /2О2(г) = Н2О(ж); Н = –285,84 кДж; (2) СаО(к) + Н2О(ж) = Са(ОН)2(к); Н = –65,06 кДж; (3)
- Для определения калия в промстоке использовали пламеннофотометрический метод. Были получены следующие результаты: 12,4; 12,8; 12,3; 12,4, 12,4, 12,8. Найдите стандартное отклонение, доверительный интервал, доверительные границы (Р=0,95)
- Содержание основного действующего вещества ранитидина в препарате Рантак (раствор для инъекций) 25 мг/мл определяют методом ВЭЖХ, измеряя площадь пиков S и Sст на хроматограммах анализируемого и стандартного растворов. Препарат Рантак содержит ратидина гидрохлорида C13H22N4O3S*HC1 (M.м. ранитидина M1 =314,40; М.м. ранитидина гидрохлорида M2=350,86).
- Рассчитать массовую долю (%) компонентов газовой смеси по данным, полученным газовой хроматографии: Следующим данным Газ S k Бензол 85 1,0 Гексан 27 1,1 Пропилен 34 1,1 Этанол 11 1,8
- Для определения содержания фенола в анализируемой воде к пробе воды объемом 200мл прибавили кислоту, избыток бромида калия и провели кулонометрическое титрование фенола электрогенерированным бромом при постоянном токе 50 мА. Для завершения реакции С6Н5ОН + 3Вr2 = С6Н2(ОН)Вr3(т) + 3НВr
- Навеску цветного сплава массой 1,811 г растворили и путем электролиза при постоянной силе тока I = 0,220 А за 40 минут выделили полностью на катоде медь и на аноде свинец в виде диоксида свинца. Определить массовую долю меди и свинца в сплаве, если выход по току составлял 100 %.
- Используя зависимость lg (I /Id-I) -E , вычислить потенциал полуволны и число электронов, участвующих в катодном процессе, по следующим данным: Бензальдегид С6Н5СНО в фосфатном буферном растворе, pH 2,75
