
Задача. По изотерме адсорбции азота рассчитайте удельную поверхность адсорбента. Площадь, занимаемая молекулой азота равна Sо= 1,62*10-19 м 2 . (Решение → 26504)
заказ№38755
Задача.
По изотерме адсорбции азота рассчитайте удельную поверхность адсорбента. Площадь, занимаемая молекулой азота равна Sо= 1,62*10-19 м 2 . Р/РS 0,05 0,10 0,15 0,20 0,25 0,30 а*10, м3 /кг 0,70 1,10 1,17 1,32 1,45 1,55
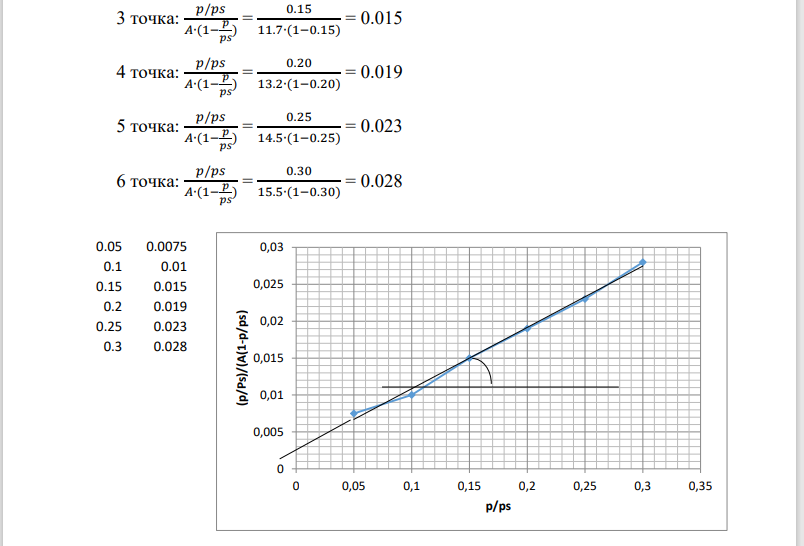
Решение: Уравнение изотермы адсорбции БЭТ широко используется для определения величины удельной поверхности адсорбентов. Изотерма адсорбции выражается прямой линией, отсекающей на оси ординат отрезок, равный 1 / АМ С , а тангенс угла ее наклона к оси абсцисс равен (С − 1) / АМ С. Согласно нашим данным, построим зависимость, сделав предварительные расчёты: 1 точка: 𝑝/𝑝𝑠 𝐴∙(1− 𝑝 𝑝𝑠 ) = 0.05 7.0∙(1−0.05) = 0.0075 2 точка: 𝑝/𝑝𝑠 𝐴∙(1− 𝑝 𝑝𝑠 ) = 0.10 11.0∙(1−0.10) = 0.010 3 точка: 𝑝/𝑝𝑠 𝐴∙(1− 𝑝 𝑝𝑠 ) = 0.15 11.7∙(1−0.15) = 0.015 4 точка: 𝑝/𝑝𝑠 𝐴∙(1− 𝑝 𝑝𝑠 ) = 0.20 13.2∙(1−0.20) = 0.019 5 точка: 𝑝/𝑝𝑠 𝐴∙(1− 𝑝 𝑝𝑠 ) = 0.25 14.5∙(1−0.25) = 0.023 6 точка: 𝑝/𝑝𝑠 𝐴∙(1− 𝑝 𝑝𝑠 ) = 0.30 15.5∙(1−0.30) = 0.028 0.05 0.0075 0.1 0.01 0.15 0.015 0.2 0.019 0.25 0.023 0.3 0.028 0 0,005 0,01 0,015 0,02 0,025 0,03 0 0,05 0,1 0,15 0,2 0,25 0,3 0,35 (p/Ps)/(A(1-p/ps) p/ps Отрезок, отсекаемый прямой на оси ординат, равен 0.003, то есть: 1 𝐴𝑚𝐶 = 0.003 Тангенс угла наклона прямой равен (так как константа С имеет большое значение): tg α = 1/Am = tg 40º = 0.73 Тогда: Am = 1/0.73 = 1.37 Уравнение для полислойной адсорбции имеет вид: В приведенном уравнении АМ - емкость монослоя, С - константа, равная е (q1− λ) / RT . Зная величину Аm, можно определить величину удельной площади по формуле: Sуд = Аm∙Na∙S0 Подставив имеющиеся данные, получим: Sуд = 1.37∙6.022∙1023∙1.62·10-19= 0.134∙102 (м2 ).



- Rp.:Calcii gluconatis 0,3 Sacchari 0,3 M.f.pulvis D.t.d N.10
- Rp.: Sol. Acidi ascorbinici 10%-50ml D.S. По 15 мл внутрь 2 раза в день.
- Каков объем 16 г, вызывающего кислотные дожди, газа диоксида серы (при нормальных условиях)? 1) Дано: m(SО2) = 16 г.
- Количественное определение препарата «Calcii chloridum» согласно ФС 42-2567-00 проводят следующим образом: около 0,8 г препарата (точная масса), отвешенные в закрытом бюксе, растворяют в воде, переносят в мерную колбу емкостью 100 мл, доводят объем раствора водой до метки и тщательно перемешивают. К 25 мл полученного раствора прибавляют 5 мл аммиачного буферного раствора, 0,1 г индикаторной смеси или 7 капель раствора кислотного хром темно-синего и титруют при энергичном перемешивании 0,05 моль/л раствором трилона Б до синего-фиолетового окрашивания.
- Вычислить при 25° ЭДС цепи Ag | AgNO3 || AgNO3,| Ag (концентрации AgNO3 0.1 н и 0.01 н соответственно). При этой температуре эквивалентная электропроводность 0.1 н AgNO3 равна 10.9 Ом-1 кэкв-1 м 2 , а для 0.01н AgNO3 она равна 12.5 Ом-1 кэкв-1м 2
- Рассчитайте объем 0,1 моль/л раствора натрия нитрита, который израсходуется на титрование парацетамола, если точная масса вещества в препарате равна 0,2456 г. Содержание парацетамола в препарате составило 99,0%.
- Рассчитайте объем 0,1 моль/л раствора натрия гидроксида, который израсходуется на титрование 0,2200 г (точная навеска) фталазола при определении его алкалиметрическим методом в среде диметилформамида. Молекулярная масса фталазола равна 403,4.
- Вычислите криоскопическую постоянную бензола, зная, что при растворении 0,0125 моль вещества в 125 г бензола температура кристаллизации его понижается на 0,512°.
- Через раствор CuSO4 пропускали ток силой 0,15 А. Число переноса Cu2+ равно 0,4. Сколько ионов меди пройдет через поперечное сечение электролита за 30 минут ?
- 100 мл раствора с массовой долей 96 % (плотность 1,84 г/мл) прибавили к 100 мл воды. Получили раствор с плотностью 1,225 г/мл.
- Рассчитать константу равновесия реакции СО2(г) + Н2(г) ↔ СО(г) + H2O(г) при температуре 850°С, если начальная концентрация СО2 составляет 1 моль/л, а Н2 - 5 моль/л и к моменту равновесия прореагировало 80 % СО2.
- Напишите полуреакции, протекающие на электродах, и суммарную реакцию при работе электрохимической цепи. Получите уравнение для ЭДС цепи.
- Константа равновесия гомогенной системы CO(к)+Н2О(г)↔СО2(г)+Н2(г) при некоторой температуре равна 1. Вычислите равновесные концентрации всех реагирующих веществ, если исходные концентрации: Сисх.(СО)=0,05 моль/л, Сисх.(Н2О)=0,2 моль/л.
- Задача. Рассчитать энергию взаимодействия сферических частиц (r=5*10-7 м) в водном растворе NaCl с концентрацией С = 0,52 моль/м3 при T=293K. Порог коагуляции этой дисперсной системы раствором NaCl равен Cкp= 15 моль/м3 .
