
Рассчитать константу равновесия превращения н-гексана в бензол при Т=250С (Решение → 34698)
Заказ №38828
Рассчитать константу равновесия превращения н-гексана в бензол при Т=250С
Решение:
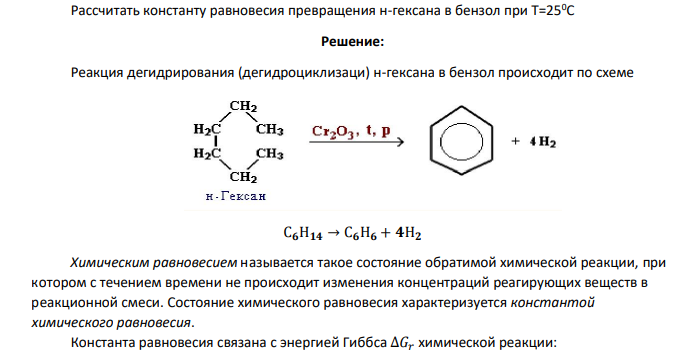
Реакция дегидрирования (дегидроциклизаци) н-гексана в бензол происходит по схеме С𝟔Н𝟏𝟒 → С𝟔Н𝟔 + 𝟒Н𝟐 Химическим равновесием называется такое состояние обратимой химической реакции, при котором с течением времени не происходит изменения концентраций реагирующих веществ в реакционной смеси. Состояние химического равновесия характеризуется константой химического равновесия. Константа равновесия связана с энергией Гиббса ∆𝐺𝑟 химической реакции: ∆𝐺𝑟 = −𝑅 ∙ 𝑇 ∙ 𝑙𝑛𝐾𝑝 (1.1) где R=8,31 Дж/(моль*К) - универсальная газовая постоянная; Т- температура процесса, К. Изменение энергии Гиббса в ходе химической реакции ∆𝐺𝑟 не зависит от пути процесса и может быть рассчитано по следствию из закона Гесса: изменение энергии Гиббса в результате химической реакции равно сумме энергий Гиббса продуктов реакции за вычетом суммы энергий Гиббса исходных веществ с учетом стехиометрических коэффициентов. В данном случае определяем энергию Гиббса реакции превращения н-гексана в бензоол при стандартных условиях Т=298К (250С) по справочным данным, принимая, что энергия Гиббса простых веществ равна нулю.

- Провести процедуру краткосрочного прогнозирования спроса на некоторую услугу (млн руб.), используя процедуру сглаживания (по пяти точкам). Таблица 1 Динамика объема спроса Месяц 1 2 3 4 5 6 7 8 9 10 11 12 Объем спроса, млн. руб. 10 15 20 15 30 25 30 40 45 50 60 65
- Раствор кальция хлорида при его содержании, указанном в соответствующей ФС, не должен давать положительной реакции на цинк ион. Как это доказать?
- Спрос фирмы монополиста описывается уравнением Qd = 80 – 2P. Общие издержки TC = 2q2 – 10q. Определите объем производства, при котором прибыль будет максимальной, и величину максимальной прибыли.
- Себестоимость производства телевизоров y (в тыс. руб.) описывается функцией 0,01 0,5 12 2 y x x , где x – объем выпускаемой продукции в месяц (тыс. ед.). Определите скорость и темп изменения себестоимости при выпуске продукции 20 тыс. ед. и 40 тыс. ед.
- Анализ диаграммы состояния двухкомпонентных систем
- Плотности жидкого и твердого олова при температуре плавления (231,9 °C) равны 6,980 г⋅см–3 и 7,184 г⋅см–3 соответственно. Энтальпия плавления олова равна 1,690 ккал⋅моль –1 .
- Какой объем раствора сульфата хрома (III) с молярной концентрацией эквивалента 0,3 моль/л потребуется для реакции с оксидом свинца (IV) массой 7,14 г в кислотной среде? Дано: Сэ(Cr2(SO4)3)=0,3 моль-экв/л m(PbO2)=7,14г
- Определите, возможна ли при Т=2000 К реакция Fe2О3(K) + 3CО(г) = 2Fe(к) + 3CО2(г) Ответ подтвердите расчетом энергии Гиббса. используя данные табл.3.
- При помощи каких реакций можно отличить находящиеся в растворе ионы
- Рассчитать прогнозное значение по методу ЭВС на основе данных, приведенных в таблице с шагом прогнозирования, равным 1, и начальной оценкой U0 = 15.
- Определение растворимости и произведения растворимости малорастворимого соединения методом кондуктометрии
- Сколько бутана нужно сжечь, чтобы приготовить 2 килограмма кипятка из льда с начальной температурой 0 0С? Дано: m(Н2О)=2 кг tк=1000С tн=00С Найти: m(C4H10) - ?
- Р. занял большую сумму денег у В. Решив избавиться от долга, Р. пригласил В. к себе на дачу и, улучив момент, накинулся на В. со спины и стал душить свою жертву. Почувствовав, что В. прекратил сопротивление, ослабел и обмяк, Р. прекратил его душить.
- Пользуясь значениями ΔG 0 образования отдельных соединений, вычислите изменение энергии Гиббса реакции СОСl2(г) = СО(г) + Сl2(г) и определите, возможно ли ее осуществление в стандартных условиях. При каких условиях возможна данная реакция?
